
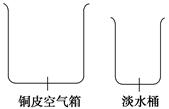
科目:高中化学 来源:不详 题型:填空题
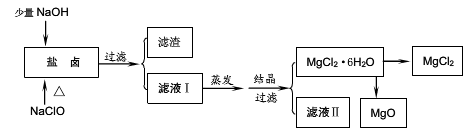
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
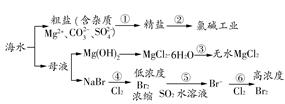
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br-,需消耗2.24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.冶金工业中,金属铁的冶炼主要采用电解法 |
| B.炼铁过程中铁的氧化物被焦炭还原生成单质铁,电解冶炼铝的过程中,阳极生成铝单质,阴极生成氧气 |
| C.炼铁的主要原料是铁矿石、焦炭、生石灰和空气,电解冶炼铝的原料是氧化铝和冰晶石 |
| D.铁、铝冶炼设备分别是炼铁高炉和铝电解槽 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水资源,不必节约 |
| B.海水淡化的主要方法有蒸馏法、电渗析法和离子交换法 |
| C.海水淡化的各种方法中,蒸馏法的成本最低 |
| D.以上说法都正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
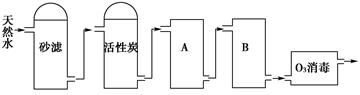
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.全部 | B.只有①②③④ |
| C.只有①②③⑤ | D.只有①②④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
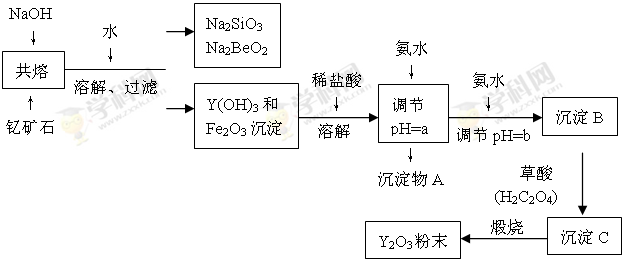
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com