
| A. | 0.1 mol溴苯中含有双键的数目为0.3NA | |
| B. | 标准状况下,22.4 L己烷中含己烷分子数目为NA | |
| C. | 1mol甲醇中含有C-H键的数目为4NA | |
| D. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA |
分析 A、溴苯中无碳碳双键;
B、标况下己烷为液体;
C、甲醇的结构简式为CH3OH;
D、求出CH4和C2H4混合物的物质的量,然后根据两者均含4个氢原子来分析.
解答 解:A、苯环不是单双键交替的结构,故溴苯中无碳碳双键,故A错误;
B、标况下己烷为液体,故不能根据气体摩尔体积来计算其物质的量和分子数目,故B错误;
C、甲醇的结构简式为CH3OH,故1mol甲醇中含3molC-H键即3NA条,故C错误;
D、标况下11.2LCH4和C2H4混合物的物质的量为0.5mol,而两者均含4个氢原子,故0.5mol混合物中含2mol氢原子即2NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1:8 | B. | 5:2 | C. | 1:5 | D. | 5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 向甲苯中滴入少量浓溴水,充 分振荡,静置 | 下层接近无色 | 说明甲苯与溴发生了 取代反应 |
| B | 向蛋白质溶液中加入适量 CuSO4溶液并充分混合 | 溶液中有沉淀析出 | 可用CuSO4溶液分离、提纯蛋白质 |
| C | 溴乙烷与NaOH水溶液混合共热后,再加入稀硝酸至溶液呈酸性,滴入硝酸银溶液 | 溶液中出现淡黄色沉淀 | 说明溴乙烷中含有溴元素 |
| D | 向适量淀粉溶液中加入少量稀硫酸,加热约5 min,冷却后再加入新制Cu(OH)2浊液并加热 | 混合液中无红色沉淀出现 | 说明淀粉没有发生水解反应生成葡萄糖 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2→Na2CO3 | B. | FeCl3→FeCl2 | C. | H2SiO3→Na2SiO3 | D. | S→SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
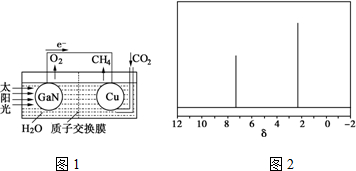 数十年来,化学工作者对碳的氧化物和氢化物做了广泛深入的研究并取得了一些
数十年来,化学工作者对碳的氧化物和氢化物做了广泛深入的研究并取得了一些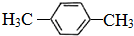 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. | A、B、C都不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
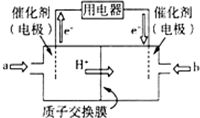 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.工业生产甲醇的常用方法是CO(g)+2H2(g)═CH3OH(g)△H<0.
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.工业生产甲醇的常用方法是CO(g)+2H2(g)═CH3OH(g)△H<0.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(HCN)+c(CN-)=0.2 mol•L-1 | B. | c(CN-)>c(HCN) | ||
| C. | c(CN-)>c(Na+) | D. | c(CN-)+c(OH-)=0.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com