
| A. | ①和③ | B. | ③ | C. | ④ | D. | 以上都不对 |
分析 中和热是强酸和强碱的稀溶液完全反应生成1mol水时放出的热量,依据概念对选项分析判断.
解答 解:①反应生成了2mol水,反应的焓变为-114.6kJ/mol,故不符合;
②反应过程中除了氢离子和氢氧根离子反应放热,硫酸钡沉淀的生成也伴随有沉淀热的变化,反应热大于-57.3kJ•mol-1,故不符合;
③一水合氨是弱电解质电离过程是吸热过程,反应热大于-57.3kJ•mol-1,故不符合;
④一水合氨和醋酸都是弱电解质电离过程是吸热过程,反应热大于-57.3kJ•mol-1,故不符合;
故选D.
点评 本题考查了中和热的概念分析判断,注意酸碱反应过程中的弱电解质电离,反应生成水的量,准确理解概念是解题关键.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
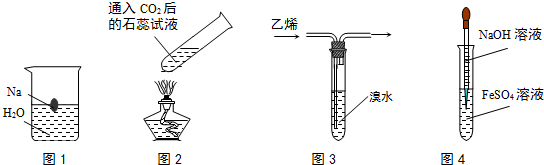
| A. | 图1中溶液颜色变化:无色→红色 | |
| B. | 图2中溶液颜色变化:红色→紫色 | |
| C. | 图3中溴水颜色变化:红棕色→无色 | |
| D. | 图4中生成的沉淀颜色变化:白色→绿色→红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下VL氨气溶解在1L水中(水的密度近似为1g/L),所得溶液的密度为ρg/mL,所配溶液的物质的量浓度c=$\frac{1000Vρ}{(17V+22400)}$ | |
| B. | 只含0.1mol、NH4+、0.1molCa2+、0.1molCO32-和0.1molCl-的溶液 | |
| C. | 质量分数为a%,物质的量浓度为c1mol/L的稀硫酸蒸发水后,其质量分数为2a%,物质的量浓度为c2mol/L,则2c1>c2 | |
| D. | 仅用1 000 mL的容量瓶、烧杯、玻璃棒、量筒、58.5 g NaCl固体和水配制1 L 1 mol/L的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含分子数相同 | B. | 质量之比为16:17 | ||
| C. | 所含氢原子的物质的量之比为3:4 | D. | 密度之比为17:16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ①②③ | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能量转化形式相同 | B. | 两极的名称相同 | ||
| C. | 负极和阴极上移向的离子类别相同 | D. | 负极和阳极上发生的反应类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:H2O<H2S<H2Se | B. | 半径:F->Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 熔点:SiO2>NaCl>CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com