
 科学家尝试用微生物电池除去废水中的有害的有机物,其原理如图所示.下列有关说法正确的是( )
科学家尝试用微生物电池除去废水中的有害的有机物,其原理如图所示.下列有关说法正确的是( )| A. | 若 1mol  转化为 1mol 苯酚转移 2mole-,则同时生成的 X 为氯气 转化为 1mol 苯酚转移 2mole-,则同时生成的 X 为氯气 | |
| B. | 用该电池电解饱和食盐水(使用情性电极的电解槽)毎产生 22.4L 的氢气,B 极上生成 0,.5molHCO3- | |
| C. | A 极为正极,B 极为负极 | |
| D. | 电池工作过程中 A 极周围溶液 pH 不断增大 |
分析 原电池工作时,阳离子向正极移动,则A是正极,正极上发生得电子的还原反应: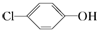 +2e-+H+═
+2e-+H+═ -OH+Cl-,B为负极,反应:CH3COO--8e-+4H2O═2HCO3-+9H+,以此解答该题.
-OH+Cl-,B为负极,反应:CH3COO--8e-+4H2O═2HCO3-+9H+,以此解答该题.
解答 解:A.A是正极,正极上发生得电子的还原反应: +2e-+H+═
+2e-+H+═ -OH+Cl-,所以若 1mol
-OH+Cl-,所以若 1mol  转化为 1mol 苯酚转移 2mole-,则同时生成的 X 为Cl-,故A错误;
转化为 1mol 苯酚转移 2mole-,则同时生成的 X 为Cl-,故A错误;
B.未指明标准状况,无法计算,故B错误;
C.原电池工作时,阳离子向正极移动,则A是正极,B为负极,故C正确;
D.A是正极,正极上发生得电子的还原反应: +2e-+H+═
+2e-+H+═ -OH+Cl-,因为B极生成氢离子移向A极,则A 极周围溶液 pH 基本不变,故D错误.
-OH+Cl-,因为B极生成氢离子移向A极,则A 极周围溶液 pH 基本不变,故D错误.
故选C.
点评 本题考查新型电池,为高频考点,题目难度不大,注意把握原电池的工作原理以及电极反应式的书写,解答本题的关键是根据物质的性质判断原电池的正负极.


科目:高中化学 来源: 题型:选择题
| A. | 人们可以利用先进的化学技术和设备制造新的原子 | |
| B. | 人们可以利用催化剂使水变成汽油 | |
| C. | 人们可以利用先进的技术和设备制造新的分子 | |
| D. | 化学科学只能通过实验来探讨物质的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 伏打电堆是由几组锌和银的圆板堆积而成,所有的圆板之间夹放着几张盐水泡过的布.图为最初的伏打电堆模型,由八组锌和银串联组成的圆板堆积而成.下列说法正确的是( )
伏打电堆是由几组锌和银的圆板堆积而成,所有的圆板之间夹放着几张盐水泡过的布.图为最初的伏打电堆模型,由八组锌和银串联组成的圆板堆积而成.下列说法正确的是( )| A. | 该原电池正极的电极方程式为:O2+4e-+4H+═2H2O | |
| B. | 电池长时间工作后,中间的布上会有白色固体颗粒生成,该固体颗粒为Ag2O | |
| C. | 当电路中转移0.2 mol电子时,消耗锌板的总质量为52 g | |
| D. | 该伏打电堆工作时,在银板附近会有Cl2放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| Ksp | 1.0×10-33 | 4.0×10-38 | 2.0×10-20 | 4.0×10-14 |
 ;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.
;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
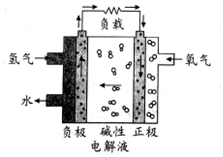
| A. | 通入氢气的电极发生氧化反应 | |
| B. | 正极的电极反应式为O2+2H2O+4e-═4OH- | |
| C. | 碱性电解液中阳离子向通入氢气的方向移动 | |
| D. | 放电过程中碱性电解液的pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
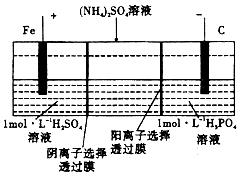
| A. | 阳极室溶液由无色变成浅绿色 | |
| B. | 当电路中通过lmol电子的电量时,阴极有0.5mol的气体生成 | |
| C. | 电解时中间室(NH4)2SO4溶液浓度下降 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释 |
| A | 液氨可用作制冷剂 | NH3的化学性质稳定,不易发生反应 |
| B | 小苏打片用于治疗胃酸过多 | Na2CO3能与盐酸反应,降低胃液的酸度 |
| C | SO2可用作葡萄酒的食品添加剂 | SO2具有漂白性,能杀菌、消毒 |
| D | Al(OH)3用作塑料等材料的阻燃剂 | 受热易分解生成Al2O3和H2O,同时吸收热量 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2mol | B. | 2.4mol | C. | 0.8mol | D. | 0.4mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com