
 .
. .
.分析 A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大.其中B的基态原子有3个不同的能级,且各能级中的电子数相等,原子核外电子排布式为1s22s22p2,故B为碳元素;A的最高正价和最低负价的绝对值相等,原子序数小于碳,故A为H元素;E的基态原子的s能级的电子总数与p能级的电子数相等,原子核外电子排布式为1s22s22p4或1s22s22p63s2,D的基态原子与B的基态原子的未成对电子数目相同,D的原子序数小于E,D原子核外电子排布只能为1s22s22p4,则D为O元素,故E为Mg,而C的原子序数介于碳、氧之间,则C为N元素;F的基态原子的3d轨道电子数是4s电子数的5倍,G的3d轨道有3个未成对电子,且F的原子序数小于G的,则F原子核外电子排布为1s22s22p63s23p63d54s1,G原子核外电子排布为1s22s22p63s23p63d74s2,故F为Cr,G为Co,据此解答.
解答 解:A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大.其中B的基态原子有3个不同的能级,且各能级中的电子数相等,原子核外电子排布式为1s22s22p2,故B为碳元素;A的最高正价和最低负价的绝对值相等,原子序数小于碳,故A为H元素;E的基态原子的s能级的电子总数与p能级的电子数相等,原子核外电子排布式为1s22s22p4或1s22s22p63s2,D的基态原子与B的基态原子的未成对电子数目相同,D的原子序数小于E,D原子核外电子排布只能为1s22s22p4,则D为O元素,故E为Mg,而C的原子序数介于碳、氧之间,则C为N元素;F的基态原子的3d轨道电子数是4s电子数的5倍,G的3d轨道有3个未成对电子,且F的原子序数小于G的,则F原子核外电子排布为1s22s22p63s23p63d54s1,G原子核外电子排布为1s22s22p63s23p63d74s2,故F为Cr,G为Co.
(1)由上述分析可知,F基态原子核外电子排布为1s22s22p63s23p63d54s1,G原子核外电子排布为1s22s22p63s23p63d74s2,处于周期表中第四周期第Ⅷ族,
故答案为:1s22s22p63s23p63d54s1;第四周期第Ⅷ族;
(2)C、N、O同周期,随原子序数增大的第一电离能呈增大趋势,但N元素2p能级容纳3个电子,处于半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能由小到大的顺序为C<O<N,
H、N、O形成的离子化合物为NH4NO3,含有的化学键有离子键、共价键,
故答案为:C<O<N;离子键、共价键;
(3)a.C2H2分子中含有C≡C三键、C-H键,含有σ键和π键,而H2O2分子为H-O-O-H,只含有σ键,故a错误;
b.C2H2常温下为气态,而H2O2常温下为液态,故b正确;
c.C2H2、H2O2均含有极性键、非极性键,C2H2是直线型对称结构,是非极性分子,而H2O2分子是展开书页形结构,属于极性分子,故c错误;
d.C2H2分子、H2O2分子含有电子总数或价电子总数不相等,不是等电子体,故d错误;
e.C2H2分子中C原子成2个σ键、没有孤对电子,杂化轨道数目为2,采取sp杂化,H2O2分子中O原子成2个σ键、含有2对孤电子对,杂化轨道数目为4,采取sp3杂化,故e错误,
故答案为:b;
(4)用电子式表示MgCl2的形成过程: ,
,
故答案为: ;
;
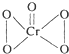
(5)Co的最高正价为+6价,而氧原子最多只能形成2个共价键,CrO5的结构式为 ,
,
故答案为: ;
;
(6)C的最低价的氢化物为NH3,通常情况下,Co2+的溶液很稳定,它与NH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为[Co(NH3)6]3+,该反应的离子方程式是:4[Co(NH3)6]2++O2+2H2O═4[Co(NH3)6]3++4OH-,1mol[Co(NH3)6]3+配离子含有6mol配位键、18molN-H键,则含有σ键数目为 24 NA,
故答案为:4[Co(NH3)6]2++O2+2H2O═4[Co(NH3)6]3++4OH-;24 NA.
点评 本题考查物质结构与性质,涉及核外电子排布、电离能、分子结构与性质等,学生要熟练掌握基础知识,并能迁移运用,难度中等.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:实验题
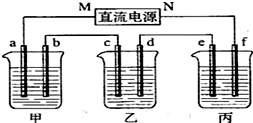
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中的溶质只有NH4Cl | |
| B. | 当溶液呈碱性时:c(NH4+)+c(H+)<c(Cl-)+c(OH-) | |
| C. | 溶液中离子浓度大小关系可能为:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 该溶液可能由pH=12的氨水与pH=2的HCl溶液等体积混合而成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②④⑥ | C. | ①③⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
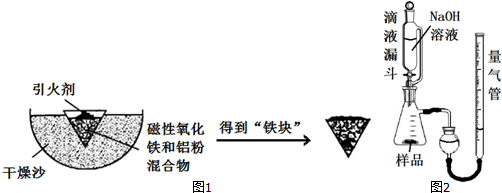

| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol-NH2中含有的电子数为0.7NA | |
| B. | 标准状况下,2.24 L乙醇中含有的C-H数目为0.5NA | |
| C. | 常温常压下,65 g Zn与足量浓H2SO4充分反应,转移电子数一定为2NA | |
| D. | 2.24 L NO与1.12 L O2充分反应所得气体中原子数目一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=10-4mol•L-1的溶液中:NH4+、K+、SO42-、NO3- | |
| B. | 无色溶液中:Na+、Cu2+、Cl-、NO3- | |
| C. | 0.1 mol•L-1AgNO3 溶液:H+、K+、SO42-、I- | |
| D. | 饱和氯水中:Cl-、Na+、NO3-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
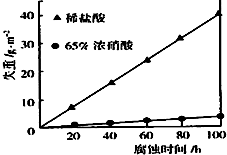 按要求回答下列问题:
按要求回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com