
| A. | ②④③① | B. | ②③① | C. | ②④③⑤① | D. | ②⑤③① |
分析 检验卤代烃中所含有的卤素原子,先使卤代烃中的卤素原子变为卤离子,在氢氧化钠水溶液中水解生成卤离子,再加入硝酸酸化,最后加入硝酸银,观察是否沉淀生成及颜色,确定含有的卤素原子,以此来解答.
解答 解:鉴定卤代烃中所含有的卤素原子,先②加入少许卤代烃试样、再④加入5mL 4mol/L NaOH溶液,然后③加热,发生水解反应生成卤素离子,再⑤加入5mL 4mol/L HNO3溶液,最后①加入AgNO3 ,观察沉淀及其颜色可确定卤素原子,所以实验顺序为:②④③⑤①;
故选C.
点评 本题考查有机物的中卤素原子检验,注意卤代烃中不含卤离子,明确卤离子的转化是解答的关键,水解后加酸至酸性为解答的易错点,题目难度不大.


 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选 项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使酸性高锰酸钾褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可使纸张变黑 |
| D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式:${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{C}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$ | |
| B. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| C. | NH4Cl的电子式: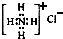 | |
| D. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③④ | C. | ④⑤ | D. | ③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐析可提纯蛋白质并保持其生理活性 | |
| B. | 油脂碱性或者酸性条件下的水解反应叫做皂化反应 | |
| C. | 打针时用75%的乙醇溶液消毒是蛋白质变性知识的应用 | |
| D. | 蛋白质、纤维素、淀粉都是高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D>A>B>C | B. | A>D>B>C | C. | D>A>C>B | D. | C>B>A>D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com