
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:

回答下列问题:
(1)A的结构简式为_________
(2)③的反应试剂和反应条件分别是________,该反应的类型是________。
(3)⑤的反应方程式为_____吡啶是一种有机碱,其作用是______。
(4)G的分子式为___________
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有____种。
【答案】 ![]() 浓硝酸、浓硫酸,并加热 取代反应
浓硝酸、浓硫酸,并加热 取代反应  吸收反应产物的HCl,提高反应转化率 C11H11O3N2F3 9种
吸收反应产物的HCl,提高反应转化率 C11H11O3N2F3 9种
【解析】考查有机物的推断与合成,(1)反应①为取代反应,A的分子式为C7H8,A为芳香烃,即A的结构简式为![]() ;(2)C和D结构简式的对比,反应③应发生硝化反应,即反应试剂和条件是浓硝酸、浓硫酸、加热;该反应类型为取代反应;(3)对比E的结构简式和G的结构简式,反应⑤发生取代反应,即F的结构简式为
;(2)C和D结构简式的对比,反应③应发生硝化反应,即反应试剂和条件是浓硝酸、浓硫酸、加热;该反应类型为取代反应;(3)对比E的结构简式和G的结构简式,反应⑤发生取代反应,即F的结构简式为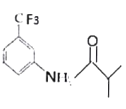 ,反应方程式为
,反应方程式为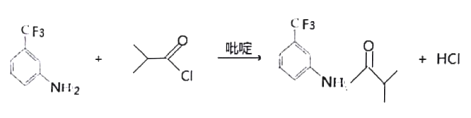 ;吡啶是一种碱,而反应⑤生成HCl,吡啶与HCl反应,提高反应转化率;(4)根据G的结构简式,推出G的分子式为C11H11O3N2F3;(5)采用定二移一的原则,-CF3和-NO2处于邻位,另一个取代基进行移动,有4种,除去G本身,有3种,-CF3和-NO2处于间位,另一个取代基进行移动,有4种位置,-CF3和-NO2处于对位,另一个取代基有2种,共有9种。
;吡啶是一种碱,而反应⑤生成HCl,吡啶与HCl反应,提高反应转化率;(4)根据G的结构简式,推出G的分子式为C11H11O3N2F3;(5)采用定二移一的原则,-CF3和-NO2处于邻位,另一个取代基进行移动,有4种,除去G本身,有3种,-CF3和-NO2处于间位,另一个取代基进行移动,有4种位置,-CF3和-NO2处于对位,另一个取代基有2种,共有9种。


科目:高中化学 来源: 题型:
【题目】根据下列事实
①由X电极、碳棒和Y的硫酸盐溶液形成的原电池,碳棒上生成一层Y金属
②Z+H2O(冷)===Z(OH)2+H2↑
③由Y和W电极组成的电池,Y电极反应为Y-e-===Y2+
可知X、Y、Z、W的金属活泼性顺序为
A.X>Z>Y>WB.Z>W>X>Y
C.Z>Y>X>WD.Z>X>Y>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是重要化工原料,在国民经济中占重要地位。工业合成氨的反应为:N2(g)+3H2(g)![]() 2NH3(g) △H<0进行如下研究:在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3) 与反应时间t的关系如下表:
2NH3(g) △H<0进行如下研究:在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3) 与反应时间t的关系如下表:
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n(H2) /mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n(NH3) /mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
(1)反应速率最快的时间段是__________
A.0min-5min B .5min-10min C.10min-15min D. 15min-20min
(2)该温度下,若向同容积的另一容器中投入的N2、H2、NH3的浓度分别为3mol/L、3mol/L、3mol/L,则此时v正 __________v逆 (填 “>”“<”或“=”)。
(3)NH3合成常见的化肥尿素【化学式为CO(NH2)2】分为三步,其中第一步为:2NH3(g)+CO2(g)![]() NH2COONH4(s) △H=-160kJ/mol, 对于这个反应,在2L等容密闭容器中充入2molNH3和1molCO2,平衡时放出128kJ的热量,NH3 的转化率为__________若反应温度不变,在该容器中充入2.8molNH3和1.4molCO2,到达平衡时。c(NH3)为__________。
NH2COONH4(s) △H=-160kJ/mol, 对于这个反应,在2L等容密闭容器中充入2molNH3和1molCO2,平衡时放出128kJ的热量,NH3 的转化率为__________若反应温度不变,在该容器中充入2.8molNH3和1.4molCO2,到达平衡时。c(NH3)为__________。
(4)以氨气代替氢气研发氨燃料电池是当前科研的一个热点。
①氨燃料电池使用的电解质溶液是4mol·L-1的KOH溶液,电池反应为: 4NH3+3O2=2N2+6H2O。该反应每消耗3.4g NH3转移的电子数目为__________;
②氨燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,然后向所得溶液中加入19.6gCu(OH)2固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为__________L。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种价电子排布为2s22p5的元素,下列有关它的描述正确的有
A. 原子序数为8
B. 在同周期元素中非金属性最强
C. 在同周期元素中,其原子半径最大
D. 在同周期元素中,元素的第一电离能最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C11H12O5)同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只有2种;③1 mol A与足量的NaHCO3反应生成1 mol CO2;④遇FeCl3溶液不显色。A有如图所示转化关系:
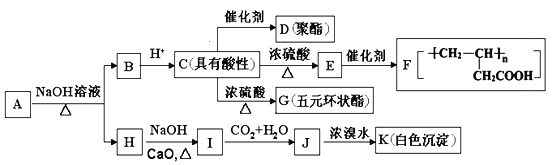
已知:
回答下列问题:
(1)E中官能团名称_____________________,H的分子式为_____________________。
(2)由C生成G的反应类型是____________________。
(3)A的结构简式为_____________________,G的结构简式为___________________。
(4)①写出C→D反应的化学方程式__________________________________________;
②写出I→J反应的离子方程式__________________________________________。
(5)C的同分异构体中能同时满足下列条件:a.能发生银镜反应,b.能发生皂化反应;c.能与Na反应产生H2,共有__________种(不含立体异构)。其中核磁共振氢谱显示为3组峰,且峰面积比为6∶1∶1的是_________________________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。
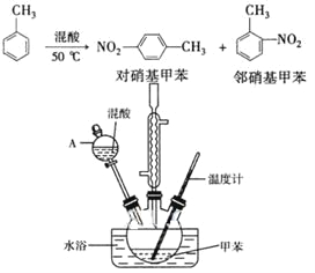
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
(1)配制混酸的方法是_______________________。反应中需不断搅拌,目的是__________________________________________。
(2)仪器A的名称是______,使用该仪器前必须进行的操作是____。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_____。
(4)分离反应后产物的方案如下:

其中,操作1的名称为______,操作2中需要使用下列仪器中的____(填序号)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(5)该实验中一硝基甲苯的产率为______(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的主要组成元素是碳、氢、氧、硫、氮,还有极少量的磷、砷、锗、镓、铟等元素,燃煤产生CxHy、SO2等大气污染物,煤的气化是高效、清洁利用煤炭的重要途径之一。回答下列问题:
(1)锗是第四周期第ⅣA族元素,其原子结构示意图为_______________________。
(2)利用煤的气化获得的水煤气(主要成分为CO、CO2和H2)在催化剂作用下可以合成绿色燃料甲醇。
已知:H2O(l)=H2O(g) △H1=+44.0kJ/mol
CO2(g)+H2(g)=CO(g)+H2O(l) △H2=-3.0 kJ/mol
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H3=-58.7 kJ/mol
写出由CO 与 H2制备 CH3OH 气体的热化学方程式___________________________________。
(3)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3,简称DMC) :
2CH3OH(g)+CO2(g)![]() CH3OCOOCH3(g)+H2O(g) ΔH4<0
CH3OCOOCH3(g)+H2O(g) ΔH4<0
①该化学反应的平衡常数表达式为K=_________________________。
②在恒温恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是_____________(填标号)。
A.v正(CH3OH)= 2v逆(H2O) B.容器内气体的密度不变
C.容器内压强不变 D.CH3OH与CO2的物质的量之比保持不变
③一定条件下分别向甲、乙丙个恒容密团容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如下表,反应过程中DMC的物质的量依度随时间变化如下图所示:
容器 | 甲 | 乙 | 丙 |
容积(L) | 0.5 | 0.5 | V |
温度(℃) | T1 | T2 | T1 |
起始量 | 1molCO2(g)2molCH3OH(g) | 1molDMC(g)1mol H2O (g) | 2molCO2(g)2molCH3OH(g) |

甲容器中,在5-15min中的平均反应速率v(CO2) =_____________。乙容器中,若平衡时n(CO2) =0.2mol,则T1________T2(填“>”“<"或”=”)。甲、丙两容器的反应达平衡时CO2的转化率:甲________丙(填“>”“<"或”=”)。
(4)一定温度下,用水吸收SO2气体时,溶液中水的电离平衡_________移动(填“向左” “向右”或“不”);若得到pH=4的H2SO3溶液,试计算溶液中 =____________。SO2可用足量小苏打溶液吸收,反应的离子方程式是_________________________________。(已知该温度下,H2SO3的电离常数:K1=4.5×10-2,K2=2.5×10-7,H2CO3的电离常数K1=8.4×10-7,K2=1.2×10-10)
=____________。SO2可用足量小苏打溶液吸收,反应的离子方程式是_________________________________。(已知该温度下,H2SO3的电离常数:K1=4.5×10-2,K2=2.5×10-7,H2CO3的电离常数K1=8.4×10-7,K2=1.2×10-10)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L容积不变的容器中,发生N2+3H2 NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol·L-1·s-1,则10 s后容器中N2的物质的量是( )
A. 1.6 mol B. 2.8 mol C. 3.6 mol D. 3.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明:H2O2具有立体结构,两个氢原子像在一本半展开的书的两页纸上,两页纸面的夹角为94°,氧原子在书的夹缝上,O—H键与O—O键之间的夹角为97°。下列说法不正确的是( )
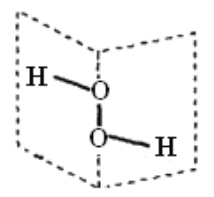
A. H2O2分子中既含极性键,又含非极性键
B. H2O2为极性分子
C. H2O2分子中的两个O原子均是sp3杂化
D. H2O2分子中既有σ键,又有π键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com