
| A. | 鸡蛋白溶液中分散质的微粒直径在1~100 nm之间 | |
| B. | 当日光从窗隙射入暗室时,可观察到一束光线 | |
| C. | 向氯化铁溶液中加入氢氧化钠溶液,产生红褐色沉淀 | |
| D. | 在河流入海处易形成沙洲 |
科目:高中化学 来源: 题型:选择题
| a | b | c | |
| A | SiO2 | Na2SiO3 | H2SiO3 |
| B | NO | NO2 | HNO3 |
| C | Fe | FeCl3 | Fe(OH)3 |
| D | Al(OH)3 | Na[Al(OH)4] | Al2O3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 各物质的质量保持不变 | B. | 各物质的浓度相等 | ||
| C. | v(逆)=v(正),正、逆反应停止 | D. | X、Y、Z的速率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、NH4+、Al3+、SO42- | B. | K+、SiO32-、Cl-、NO3- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、Fe3+、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
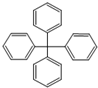
| A. | 其分子式为C25H20 | |
| B. | 分子内的所有碳原子可能共平面 | |
| C. | 完全燃烧生成CO2和H2O的物质的量之比为5:2 | |
| D. | 此分子的一氯代物有三种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三氧化铬作还原剂 | B. | 乙醇作还原剂 | ||
| C. | CrO3中Cr被氧化 | D. | 乙醇发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
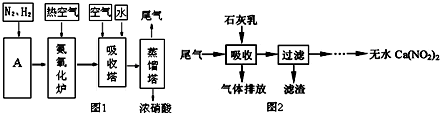
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com