
| A. | K+.Al3+.Cl-.NO3- | B. | K+.Fe3+.Cl-.SiO32- | ||
| C. | H+.Fe2+.SO42-.Br2 | D. | K+.Ag+.NH3•H2O.NO3- |
分析 A.四种离子之间不发生反应,在溶液中能够共存;
B.铁离子与硅酸根离子发生双水解反应生成硅酸和氢氧化铁沉淀;
C.溴具有强氧化性,能够将亚铁离子氧化成铁离子;
D.银离子与一水合氨发生反应.
解答 解:A.K+、Al3+、Cl-、NO3-之间不反应,在溶液中能够大量共存,故A正确;
B.Fe3+、SiO32-之间发生双水解反应,在溶液中不能大量共存,故B错误;
C.Fe2+、Br2之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.Ag+、NH3•H2O之间发生反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 碘-131原子核外有5个电子层 | |
| B. | 碘-131原子的最外层有7个电子 | |
| C. | 具有放射性的碘-131原子比普通碘-127原子多4个中子 | |
| D. | 131I2与127I2互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与氢气反应的难易程度 | B. | 氢化物的熔沸点 | ||
| C. | 非金属性的强弱 | D. | 氢化物稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,BA2的结构式是:S=C=S.
,BA2的结构式是:S=C=S.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 分子式 | 熔点℃ | 沸点℃ | 密度g•cm-3 | 水溶性 |
| A | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
| B | C4H8O2 | -84 | 97 | 0.90 | 可溶 |
| A. | 萃取 | B. | 升华 | C. | 分馏 | D. | 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 >H2CO3>
>H2CO3> >HCO3-,综合考虑反应物的转化率和原料成本等因素,将
>HCO3-,综合考虑反应物的转化率和原料成本等因素,将 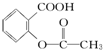 转变为
转变为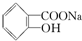 的最佳方法是( )
的最佳方法是( )| A. | 与足量的NaOH溶液共热后,再通入足量CO2 | |
| B. | 与足量的NaOH溶液共热后,再加入适量H2SO4 | |
| C. | 与稀H2SO4共热后,加入足量的NaOH溶液 | |
| D. | 与稀H2SO4共热后,加入足量的Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
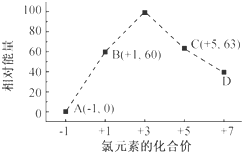 元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.
元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素组 | 例外元素 | 其他元素所属类型的编号 |
| (1)S、N、Na、Mg | N | ③ |
| (2)P、Sb、Si、As | Si | ④ |
| (3)Rb、B、Br、Fe | Fe | ① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com