
 .
. 分析 (1)烷烃命名时,要选最长的碳链为主链,从离支链近的一端给主链上碳原子编号,写出支链名称和位置,由简到繁同基合并,最后写主链名称,据此分析;
(2)苯与溴发生取代反应生成溴苯和HCl;
(3)分子中含有一个碳碳双键,为烯烃,设分子式为CnH2n,结合M=84可计算分子式,结合分子中只有一种类型的氢原子,则结构对称来推断结构简式;
解答 解:(1)烷烃命名时,要选最长的碳链为主链,故主链上有5个碳原子,故为戊烷,从离支链近的一端给主链上碳原子编号,故在2号和3号碳原子上各有一个甲基,故名称为2,3-二甲基戊烷,
故答案为:2,3-二甲基戊烷;
(2)苯与溴发生取代反应生成溴苯和HCl,该反应为C6H6+Br2$\stackrel{Fe}{→}$C6H5Br+HBr,
故答案为:C6H6+Br2$\stackrel{Fe}{→}$C6H5Br+HBr;
(3)含有1个碳碳双键,则A应为烯烃,设分子式为CnH2n,相对分子质量为84,则有14n=84,n=6,A的一氯取代产物只有一种说明分子中只有一种类型的氢,说明结构对称,即双键C上的4个H均被甲基取代,其结构简式应为 ,
,
故答案为: .
.
点评 本题考查了常见有机物的命名、化学方程式的书写、同系物与同分异构体的判断,题目难度中等,试题涉及的题量过大,知识点较多,充分考查了学生对书写知识的掌握情况.


科目:高中化学 来源: 题型:选择题
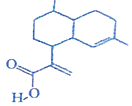
| A. | 该物质属于芳香族化合物 | B. | 该物质易溶于水 | ||
| C. | 能发生取代反应和加成反应 | D. | 分子中所有碳原子可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
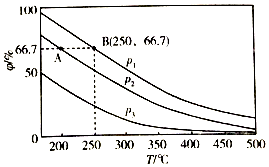 氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)?2NH3(g)△H.
氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)?2NH3(g)△H.| H-H | N-H | N-N | N |
| 435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知五种短周期元素在周期表中的相对位置如表所示.
已知五种短周期元素在周期表中的相对位置如表所示.| a | |||||
| b | |||||
| c | d | e |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
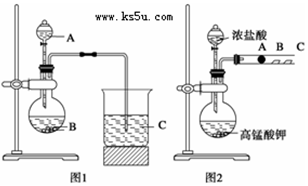
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数:a>b | B. | 离子半径:r(aX+)>r(bY-) | ||
| C. | X、Y可形成XY2型化合物 | D. | 原子半径:r(Y)>r(X) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 杜绝化石燃料的使用,从源头上解决问题 | |
| B. | 减少燃料燃烧产生的热量损耗的技术,提高燃料利用率的措施 | |
| C. | 防止燃料燃烧造成环境污染的方法 | |
| D. | 通过化学方法把化石燃料转化成洁净燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
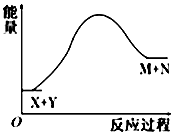
| A. | X的能量一定低于M的能量,Y的能量一定低于N的能量 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | X和Y的总能量一定低于M和N的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com