
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热,须看反应物和生成物所具有的总能量的相对大小 | |
| D. | 金刚石比石墨稳定 |
分析 A.吸热反应实质是反应物所具有的总能量低于生成物所具有的总能量;
B.一个化学反应发生的条件与反应的热效应无关;
C.化学反应中生成物总能量不等于反应物的总能量,反应前后的能量差值为化学反应中的能量变化;
D.金刚石比石墨能量高.
解答 解:A.需要加热才能发生的反应不一定是吸热反应,如铝热反应需要在高温下发生,但是放热反应,故A错误;
B.放热的反应在常温下不一定很容易发生,如:铝热反应2 Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe是放热反应,但需在高热条件下以保证足够的热量引发氧化铁和铝粉反应,故B错误;
C.放热反应是指:反应物所具有的总能量高于生成的总能量,在反应中会有一部分能量转变为热能的形式释放,反之,就是吸热反应,故C正确;
D.金刚石比石墨能量高,能量越低越稳定,故D错误.
故选C.
点评 本题考查化学反应的条件与化学反应的热效应间的关系,需正确理解放热吸热的本质,是解题的关键,难度不大.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
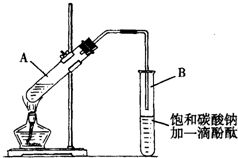 已知下列数据:
已知下列数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙 醇 | -117.0 | 78.0 | 0.79 |
| 乙 酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | -- | 338.0 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH3和CH3CH=CHCH3 | B. | CH3CH=CHCH3和 CH3C≡CCH3 | ||
| C. | CH3CH=CHCH3和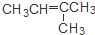 | D. | CH3CH2CH2OH和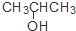 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | B. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(O{H}^{-})}$ | C. | n(OH-)和c(H+) | D. | c(H+)和c(OH-)的乘积 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com