
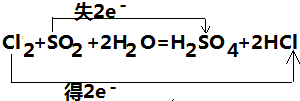 ,
,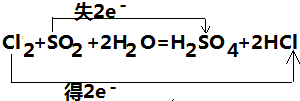 .
.


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
| A、平衡时,物质的量之比n(A):n(B):n(C)=2:11:4 |
| B、x值等于3 |
| C、A的转化率为20% |
| D、B的平均反应速率为0.4 mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在上述反应中,电子从氧化剂转移到还原剂 |
| B、物质甲可能是KMnO4 |
| C、反应中若产生3.0g气体,则转移电子数约为0.3×6.02×1023 |
| D、氧化过程的反应式一定为Cu2O-2e-+2H+═2Cu2++H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、易溶于水 | B、难溶于水 |
| C、属于硅酸盐 | D、属于复盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔质量:g |
| B、气体摩尔体积:L?mol-1 |
| C、密度:g?mL-1 |
| D、物质的量浓度:mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com