
【题目】一定温度下在容积恒定的密闭容器中,进行可逆反应:A(s)+2B(g) ![]() C(g)+D(g),当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
C(g)+D(g),当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
A.容器内气体的压强
B.混合气体的总物质的量
C.A的物质的量浓度
D.混合气体的平均相对分子质量不再变化
【答案】D
【解析】A.容器容积不变,反应前后气体的物质的量不变,容器内气体的压强始终不变,故压强不变,不能说明到达平衡状态,A不符合题意;
B.反应前后气体的物质的量不变,混合气体的总物质的量不变,不能说明到达平衡状态,B不符合题意;
C. 反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,A为固体不影响化学平衡状态,不能说明该反应达到平衡状态,C不符合题意;
D.反应前后气体的物质的量不变,随反应进行,混合气体的质量增大,混合气体的平均相对分子质量增大,平均相对分子质量不变,说明到达平衡状态,D符合题意;
所以答案是:D
【考点精析】解答此题的关键在于理解化学平衡状态的判断的相关知识,掌握状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等.


科目:高中化学 来源: 题型:
【题目】下列实验事故的处理方法正确的是( )
A.不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦
B.实验桌上的酒精灯倾倒了燃烧起来,应立即用湿布扑灭
C.皮肤上溅有较多的浓硫酸,应立即用水冲洗
D.配制硫酸溶液时,可先在量筒中加入一定体积水,再在搅拌条件下慢慢加入浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂操作可行的是( )
A.通过浓硫酸除去SO2中的H2OB.通过灼热的CuO除去H2中的CO
C.通过灼热的镁粉除去N2中的O2D.通过碱石灰除去O2中的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于钠的化学性质叙述:①钠与水剧烈反应生成氢氧化钠和氢气;②钠在空气中燃烧时生成白色固体过氧化钠;③钠与盐酸反应时先与酸反应,过量的钠再与水反应;④钠是金属,不溶于水也不和水反应;⑤钠可从硫酸铜溶液中置换出铜。正确的是( )
A.④⑤B.②③C.①②D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸广泛存在于苹果等水果的果肉中是一种常用的食品添加剂。经测定,草果酸的相对分子质量为134,所含各元素的质量分数为w(C)=35.82%,w(H)=4.48%、w(O)=59.70%。其中存在5种不同化学环境的H原子。以乙烯为原料人工合成草果酸的线路如图所示:
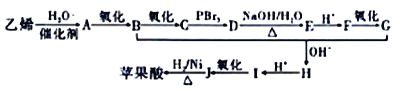
已知:①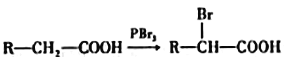
②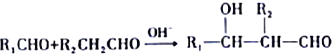
请回答下列问题:
(1)苹果酸的分子式为_______,B物质的名称为_______。F中含有的官能团名称是_______。
(2)G+B→H的反应类型是____________。I 的结构简式为___________________。
(3)D→E反应的化学方程式为________________________________。
(4)1mol苹果酸能与________molNaHCO3完全反应,能与足量的Na反应生成_______LH2(标况下)。
(5)与苹果酸含有相同种类和数量的官能团的同分异构体的结构简式为_________;其所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是__________(填序号)。
a. 元素分析仪 b.红外光谱仪 c. 质谱仪 d.核磁共振仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,向20mL0.1mol·L-1MOH溶液中滴加0.1mol·L-1CH3COOH溶液,所得溶液的pH及导电能力变化如图所示。下列叙述正确的是( )
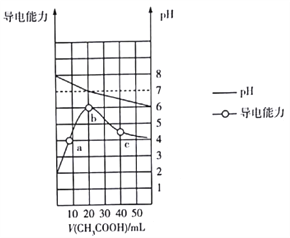
A. MOH是强电解质 B. b点对应的盐不水解
C. 水的离子积Kw:b>c>a D. c点溶液中c(CH3COO-)>c(M+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了解决目前存在的世界性能源危机,新的替代能源主要包括( )
①核能 ②柴草 ③焦碳 ④太阳能 ⑤氢能 ⑥液化石油气 ⑦水煤气 ⑧天然气.
A.②③⑥⑦
B.①④⑤
C.③⑥⑦⑧
D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素在元素周期表中的位置如图所示。
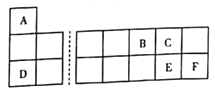
回答下列问题:
(1)在周期表中,E位于第_____________周期第_____________族。
(2)A、B能组成既含极性键又含非极性键的化合物,其电子式为_____________。
(3)在E、F的气态氢化物中,热稳定性较强的是_____________(填化学式,下同),还原性较强的是_______________。
(4)A、C、D、E组成两种酸式盐X、Y,将X、Y溶液混合发生复分解反应,写出离子方程式:________________________________________________________。
(5)常用(BA4)2E2C8检验废水中的Mn2+,若观察到无色溶液变紫红色,可判断废水中含Mn2+,还原产物与盐酸酸化的BaCl2溶液混合产生白色沉淀。写出无色溶液变紫红色溶液的离子方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是丁烷裂解的实验流程:(提示:丁烷在一定条件下裂解的可能方程式为:C4H10![]() C2H6+C2H4, C4H10
C2H6+C2H4, C4H10![]() CH4+C3H6)
CH4+C3H6)
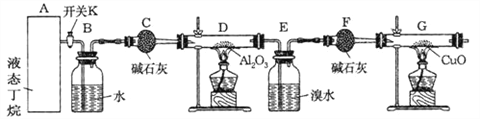
连接好装置后,需进行的实验操作有:
①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
(1)这三步操作的先后顺序依次是_______________________(填序号)
(2)写出甲烷与氧化铜反应的化学方程式______________________
(3)若对E装置中的混合物(溴水足量),再按以下流程实验:
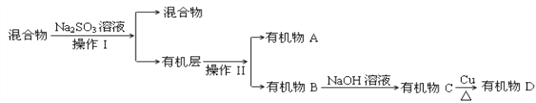
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ________Ⅱ________,Na2SO3溶液的作用是(用离子方程式表示)________________________________________________________.
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式_____________________.
(4)假定丁烷完全裂解,当(E+F)装置的总质量比反应前增加了0.7 g, G装置的质量减少了1.76 g,则丁烷的裂解产物中甲烷和乙烷的物质的量之比 n(CH4): n(C2H6)=__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com