
关于右图电化学装置中的电极名称、材料及反应均可能正确的是
A.阴极(Cu片):2Cl--2e-=Cl2↑
B.正极(石墨棒):Fe3++e-=Fe2+
C.阳极(Cu片):4OH--4e-=2H2O+O2↑
D.负极(Fe钉):Fe-3e-=Fe3+
 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
B.CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大
C.Ca(HCO3)2溶液与过量NaOH溶液反应可得到Ca(OH)2
D.25 ℃时Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钾是工业生产和实验室的重要氧化剂。工业上常用铬铁矿(主要成分为FeO·Cr2O3,以及SiO2、Al2O3等杂质)为原料生产。实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下:

图K52
反应器中主要发生的反应为
Ⅰ.FeO·Cr2O3+NaOH+KClO3→Na2CrO4+Fe2O3+H2O+KCl(未配平);
Ⅱ.Na2CO3+SiO2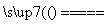 Na2SiO3+CO2↑;
Na2SiO3+CO2↑;
Ⅲ.Al2O3+2NaOH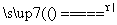 2NaAlO2+H2O。
2NaAlO2+H2O。
在步骤③中将溶液的pH调节到7~8,可以将SiO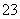 和AlO
和AlO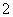 转化为相应的沉淀除去。
转化为相应的沉淀除去。
(1)在反应Ⅰ中氧化剂是________,若有245 g KClO3参加反应,则转移的电子数为______________________。
(2)反应器中生成的Fe2O3又可和Na2CO3反应得到一种摩尔质量为111 g/mol的化合物,该化合物能剧烈水解,在操作②中生成沉淀而除去。写出生成该化合物的化学反应方程式:________________________________。
(3)操作④的目的是将CrO 转化为Cr2O
转化为Cr2O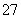 ,其现象为____________________,离子方程式为________________________________________________________________________
,其现象为____________________,离子方程式为________________________________________________________________________
________________________________________________________________________。
(4)请选用合适的方法进一步提纯粗产品重铬酸钾______(填字母)。
A.重结晶 B.萃取分液
C.蒸馏
(5)分析产品中K2Cr2O7的纯度是利用硫酸酸化的K2Cr2O7将KI氧化成I2,然后利用相关物质测出I2的量从而获得K2Cr2O7的量。写出酸化的K2Cr2O7与KI反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制乙烯时,常因温度过高而发生副反应,使部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑。
(1)请用表中编号为①、②、③、④的装置设计一个实验,以验证上述反应混合气体中含CO2、SO2和水蒸气。用装置的编号表示装置的连接顺序(按产物气流从左到右顺序):________→________→
________→________。
(2)实验时装置①中A瓶的现象是________,原因是________。B瓶中的现象是________,B瓶溶液的作用是________。若C瓶中品红溶液不褪色,说明________。
(3)装置③中加的固体药品是________,以验证混合气体中有________。装置②中盛的溶液是________,以验证混合气体中的________。
(4)装置①在整套装置中所放位置的理由是____________。
| 编号 | ① | ② | ③ | ④ |
| 装置 |
|
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应的叙述正确的是
A.铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应
B.NH3+H3O+=NH4++H2O说明结合H+的能力:H2O>NH3
C.FeCl2、Fe(OH)3均可通过化合反应制得
D.分子式为C2H4O2的化合物只能电离,不能水解
查看答案和解析>>
科目:高中化学 来源: 题型:
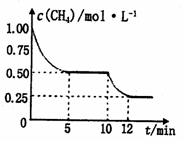
在密闭容器中进行反应CH4(g)+H2O(g)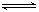 CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示,下列判断正确的是
CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示,下列判断正确的是
A.10 min时,改变的外界条件可能是减小压强
B.0~5 min内,v(H2)=0.1 mol/(L·min)
C.恒温下,缩小容器体积,平衡后c(H2)减小
D.12 min时,反应达平衡,气体的平均摩尔质量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式为( )
A.硫化亚铁溶于稀硝酸中:FeS+2H+===Fe2++H2S↑
B.NH4HCO3溶于过量的NaOH溶液中:
HCO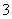 +O
+O H-===CO
H-===CO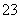 +H2O
+H2O
C.少量CO2通入硅酸钠溶液中:
SiO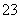 +2CO2+2H2O===H2SiO3↓+2HCO
+2CO2+2H2O===H2SiO3↓+2HCO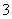
查看答案和解析>>
科目:高中化学 来源: 题型:
无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式__________________________________________
________________________________________________________________________。
(2)某无色溶液只含有下列8种离子中的某几种:Na+、H+、Mg2+、Ag+、Cl-、OH-、HCO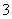 、NO
、NO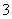 。已知该溶液可与Al2O3反应,则:
。已知该溶液可与Al2O3反应,则:
①该溶液与Al2O3反应后有Al3+生成,则原溶液中一定含有________,一定不会含有大量的________。
②该溶液与Al2O3反应后有AlO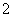 生成,则原溶液中一定含有________,可能含有大量的________。
生成,则原溶液中一定含有________,可能含有大量的________。
③写出该溶液与Al2O3反应生成AlO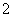 的离子方程式
的离子方程式
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向苏打和小苏打溶液中分别加入盐酸 | 均冒气泡 | 两者均能与盐酸反应 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3·H2O能大量共存 |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液 显紫红色 | 氧化性:Fe3+>I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com