
【题目】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是_____(填字母序号)
A.Fe B.FeO C.Fe3O4 D.Fe2O3
(2)现代利用铁的氧化物循环分解水制氢气的过程如下图所示。整个过程与温度密切相关,当温度低于570℃时,Fe3O4(s)和CO(g)反应得到的产物是Fe(s)和CO2(g),阻碍循环反应的进行。

①已知:Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g) ΔH1=+19.3kJ·mol-1
3FeO(s)+CO2(g) ΔH1=+19.3kJ·mol-1
3FeO(s)+H2O(g)![]() Fe3O4(s)+H2(g) ΔH2=-57.2kJ·mol-1
Fe3O4(s)+H2(g) ΔH2=-57.2kJ·mol-1
C(s)+CO2(g)![]() 2CO(g) ΔH3=+172.4kJ·mol-1
2CO(g) ΔH3=+172.4kJ·mol-1
铁氧化物循环裂解水制氢气总反应的热化学方程式是_________________。
②下图表示其他条件一定时,Fe3O4(s)和CO(g)反应达平衡时CO(g)的体积百分含量随温度(T)的变化关系。
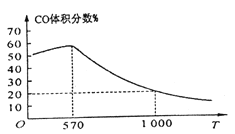
i. 当温度低于570℃时,对于反应Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g) ,温度降低,CO的转化率_____ (填“增大”、“减小”或“不变”)。
3Fe(s)+4CO2(g) ,温度降低,CO的转化率_____ (填“增大”、“减小”或“不变”)。
ii. 当温度高于570℃时,随温度升高,反应Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g)平衡常数的变化趋势是______(填“增大”、“减小”或“不变”);1000℃时,该反应的化学平衡常数的数值是__________。
3FeO(s)+CO2(g)平衡常数的变化趋势是______(填“增大”、“减小”或“不变”);1000℃时,该反应的化学平衡常数的数值是__________。
(3)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是_____________。
②基于普鲁士蓝合成原理可检测食品中CN-,方案如下:
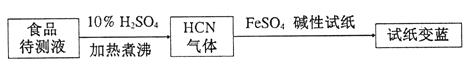
若试纸变蓝则证明食品中含有CN-,请解释检测时试纸中FeSO4的作用____________。
【答案】 C C(s)+H2O(g)=H2(g)十CO(g) ΔH=+134.5kJ/mo1 增大 增大 4 3[Fe(CN)6]4-+ 4Fe3+= Fe4[Fe (CN)6]3↓ 碱性条件下,Fe2+与CN-结合生成[Fe (CN)6]4-,Fe2+被空气中O2氧化生成Fe3+,Fe3+与[Fe(CN)6]4-反应生成普鲁士蓝使试纸显蓝色
【解析】(1)古代中国四大发明之一的司南是由天然磁石制成的,磁铁成分主要是四氧化三铁,答案选C;(2)①Ⅰ.Fe3O4(s)+CO(g)3FeO(s)+CO2(g)△H1═+19.3kJmol-1
Ⅱ.3FeO(s)+H2O(g)Fe3O4(s)+H2(g)△H2═-57.2kJmol-1
Ⅲ.C(s)+CO2(g)2CO(g)△H3═+172.4kJmol-1
依据盖斯定律计算Ⅰ+Ⅱ+Ⅲ得到铁氧化物循环裂解水制氢气总反应的热化学方程式;C(s)+H2O(g)═H2(g)+CO(g)△H═+134.5 kJmol-1;②i. 根据图中信息可知,当温度低于570℃时,对于反应Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2(g),温度降低,CO的体积分数降低,平衡正向移动,CO的转化率增大;ii.当温度高于570°C,随温度升高,反应Fe3O4(s)+CO(g)3FeO(s)+CO2(g)平衡正向进行,平衡常数的变化趋势增大,1000℃时CO体积分数为20%,结合三行计算列式计算得到平衡浓度,设起始浓度CO为1mol/L,消耗CO浓度为x
3Fe(s)+4CO2(g),温度降低,CO的体积分数降低,平衡正向移动,CO的转化率增大;ii.当温度高于570°C,随温度升高,反应Fe3O4(s)+CO(g)3FeO(s)+CO2(g)平衡正向进行,平衡常数的变化趋势增大,1000℃时CO体积分数为20%,结合三行计算列式计算得到平衡浓度,设起始浓度CO为1mol/L,消耗CO浓度为x
Fe3O4(s)+CO(g)3FeO(s)+CO2(g)
起始量(mol/L) 1 0
变化量(mol/L) x x
平衡量(mol/L) 1-x x
![]() =20%,解得:x=0.8mol/L,K=
=20%,解得:x=0.8mol/L,K=![]() =4;(3)①[Fe(CN)6]4-和Fe3+反应生成Fe4[Fe (CN)6]3蓝色沉淀,反应的离子方程式为:3[Fe(CN)6]4-+ 4Fe3+= Fe4[Fe (CN)6]3↓;②基于普鲁士蓝合成原理可检测食品中CN-,碱性条件下,Fe2+与CN-结合生成[Fe(CN)6]4-;Fe2+被空气中O2氧化生成Fe3+;[Fe(CN)6]4-与Fe3+反应生成普鲁士蓝使试纸显蓝色。
=4;(3)①[Fe(CN)6]4-和Fe3+反应生成Fe4[Fe (CN)6]3蓝色沉淀,反应的离子方程式为:3[Fe(CN)6]4-+ 4Fe3+= Fe4[Fe (CN)6]3↓;②基于普鲁士蓝合成原理可检测食品中CN-,碱性条件下,Fe2+与CN-结合生成[Fe(CN)6]4-;Fe2+被空气中O2氧化生成Fe3+;[Fe(CN)6]4-与Fe3+反应生成普鲁士蓝使试纸显蓝色。


科目:高中化学 来源: 题型:
【题目】H2(g)+I2(g)2HI(g)已经达到平衡状态的标志是( )
①c(H2)=c(I2)=c(HI)
②c(H2):c(I2):c(HI)=1:1:2
③c(H2)、c(I2)、c(HI)不再随时间而改变
④单位时间内生成nmolH2的同时生成2nmolHI
⑤单位时间内生成n mol H2的同时生成n mol I2
⑥反应速率v(H2)=v(I2)= ![]() v(HI)
v(HI)
⑦一个H﹣H键断裂的同时有两个H﹣I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
条件一定,混合气体的平均相对分子质量不再变化.
A.5项
B.4项
C.3项
D.2项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法与社会可持续发展理念相符合的是
A.推广一次性塑料袋的使用
B.应用高效洁净的能源转换技术
C.加快化石燃料的开采与使用
D.大量开采地下水以满足工业生产需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,有关说法正确的是
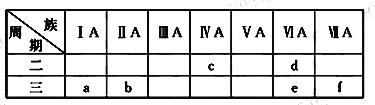
A. e的氢化物比d的氢化物稳定
B. a、b、e三种元素的原子半径:e>b>a
C. c、e、f的最高价氧化物对应的水化物的酸性依次增强
D. 六种元素中,c元素单质的化学性质最活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识解答问题:
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,则该反应的热化学方程式应为
(2)已知下列各物质的键能:N≡N 946kJ/mol、H﹣H 436kJ/mol、N﹣H 391kJ/mol,写出合成氨的热化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示: 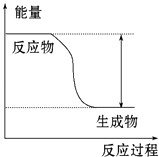
(1)该反应为反应(填“吸热”或“放热”).
(2)若要使该反应的反应速率加快,下列措施可行的是(填字母).
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为(填“正”或“负”)极.铜片上的现象为该极上发生的电极反应为 , 外电路中电子由极(填“正”或“负”,下同)向极移动.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物CH2 = CHCH2 CHO,回答下列问题:
(1)含有的官能团名称为____________________。
(2)该有机物的核磁共振氢谱有_______个峰。
(3)该有机物最多能和_______molH2发生加成反应。写出反应的化学方程式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列有关说法不正确的是( )
A.“霾尘积聚难见路人”,雾霾所形成的溶胶能产生丁达尔效应
B.“青蒿一握,以水二升渍,绞取汁”,上述对青蒿素的提取过程属于化学变化
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com