
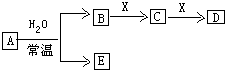
 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去).
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去). ;
;分析 (1)若A为黄绿色气体单质,则A为Cl2,与水反应生成HCl和HClO,C为无色无味能使澄清石灰水变浑浊的气体,则C为CO2,根据B、C、D的转化关系可知,B为HCl,X为Na2CO3,D为NaHCO3,则E为HClO,据此答题;
(2)若A为淡黄色固体粉末,则A为Na2O2,X为一种常见的非金属单质,根据B、C、D的转化关系可知,B为O2,X为C,则C为CO2,D为CO,所以E为NaOH,据此答题.
解答 解:(1)若A为黄绿色气体单质,则A为Cl2,与水反应生成HCl和HClO,C为无色无味能使澄清石灰水变浑浊的气体,则C为CO2,根据B、C、D的转化关系可知,B为HCl,X为Na2CO3,D为NaHCO3,则E为HClO,
①A为Cl2,A和水反应的化学方程式为Cl2+H2O?HCl+HClO,
故答案为:Cl2+H2O?HCl+HClO;
②C为CO2,C的电子式为  ,
,
故答案为: ;
;
③向Na2CO3溶液中通入Cl2,可制得某种生产和生活中常用的漂白、消毒的物质应为NaClO,同时有D生成NaHCO3,该反应的化学方程式是Cl2+2Na2CO3+H2O=NaClO+NaCl+2NaHCO3,
故答案为:Cl2+2Na2CO3+H2O=NaClO+NaCl+2NaHCO3;
(2)若A为淡黄色固体粉末,则A为Na2O2,X为一种常见的非金属单质,根据B、C、D的转化关系可知,B为O2,X为C,则C为CO2,D为CO,所以E为NaOH,
①A为Na2O2,A和水反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
②X为C,已知X的燃烧热为393.5kJ/mol,则X燃烧的热化学方程式为:C(s)+O2(g)=CO2(g),△H=-393.5kJ/mol①;D为CO,D的燃烧热为283.0kJ/mol,所以D燃烧的热化学方程式为:2CO(g)+O2(g)=2CO2(g),△H=-566.0kJ/mol②,将①-$\frac{1}{2}$②可得CO2与C的反应,此时△H=-393.5kJ/mol-$\frac{1}{2}$(-566.0kJ/mol)=-110.5kJ/mol<0,所以是 放热反应,
故答案为:C(s)+O2(g)=CO2(g),△H=-393.5kJ/mol;放热;
③向500mol 2mol/L的NaOH溶液即含1molNaOH中通入0.8mol的CO2气体,恰好完全反应,该反应的离子方程式是CO2+2OH-=H2O+CO32-、CO2+OH-=HCO3-,
故答案为:CO2+2OH-=H2O+CO32-、CO2+OH-=HCO3-.
点评 本题考查无机物的推断,是高考中的常见题型,试题综合性强,难度较大,有利于培养学生的逻辑推理能力和抽象思维能力,提高学生分析问题、以及灵活运用基础知识解决实际问题的能力.做好本题的关键之处在于把握好常见物质的性质以及有关转化,并能结合题意具体问题、具体分析即可.


科目:高中化学 来源: 题型:多选题
| A. | pH=3的H2SO4溶液中:c(H+)=10-3mol•L-1 | |
| B. | 呈中性的醋酸和醋酸钠的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 在Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 氯化铵溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
已知某可逆反应mA(g)+nB(g)?pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )| A. | T1<T2 p1>p2 m+n>p 放热反应 | B. | T1>T2 p1<p2 m+n>p 吸热反应 | ||
| C. | T1<T2 p1>p2 m+n<p 放热反应 | D. | T1>T2 p1<p2 m+n<p 吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①③④⑤⑥ | C. | ①②③⑤⑥ | D. | 只有①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 每个白藜芦醇分子中含有6个氢分子 | |
| B. | 白藜芦醇由碳、氢、氧三种元素组成 | |
| C. | 白藜芦醇的相对分子质量为228 | |
| D. | 白藜芦醇中碳、氢、氧三种元素的质量比为14:12:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com