
 KOCN+2KCl+H2O。被氧化的元素是___________。
KOCN+2KCl+H2O。被氧化的元素是___________。 CO2+N2+KCl+H2O
CO2+N2+KCl+H2O
 KOCN+2KCl+H2O反应中,氯元素价态降低,H、N、O、K四种元素的价态没变,只有碳元素的价态升高,故被氧化的为碳元素。
KOCN+2KCl+H2O反应中,氯元素价态降低,H、N、O、K四种元素的价态没变,只有碳元素的价态升高,故被氧化的为碳元素。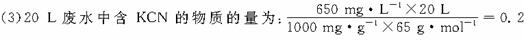
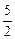 ="0.5" mol,即35.5 g。
="0.5" mol,即35.5 g。

科目:高中化学 来源:不详 题型:计算题
| a、b的关系 | Fe2+的物质的量浓度(mol/L) |
| a≤22.4b | ①___ |
| ②_____ | 0 |
| 22.4b≤a≤33.6b | ③____ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 □Cu2++□Fe2++□( )+□SO42-
□Cu2++□Fe2++□( )+□SO42-查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由反应①可推知:CH4 ( g ) + 4NO2 ( g ) =" 4NO" ( g ) + CO2 ( g ) + 2H2O ( l) ; △H>一574 kJ·mol-1 |
| B.反应①②转移的电子数相同 |
| C.若用标准状况下 4.48LCH4还原 NO2至 N2,放出的热量为 173.4kJ。 |
| D.若用标准状况下 4.48LCH4还原 NO2至 N2,整个过程中转移的电子总数为1.60 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 改变的条件 | 平衡移动的方向 | 平衡移动的过程 |
| 增大反应物的浓度 | ______ | 反应物的浓度______ |
| 减小压强 | ______ | 体系的压强逐渐______ |
| 升高温度 | ______ | 体系的温度逐渐______ |
| 使用合适的催化剂 | ______ | 速率______ 达平衡所需时间______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Si3N4+6CO。下列叙述正确的是( )
Si3N4+6CO。下列叙述正确的是( )| A.在氮化硅的合成反应中,N2是还原剂,SiO2是氧化剂 |
| B.上述反应中每生成1 mol Si3N4,N2得到12 mol电子 |
| C.若已知上述反应为放热反应,升高温度,其平衡常数增大 |
| D.若使压强增大,上述平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2∶15 | B.1∶6 | C.2∶3 | D.16∶25 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com