
将NO2装入带活塞的密闭容器中,当反应2NO2(g)N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是 ( )。
A.升高温度,气体颜色加深,则此反应为吸热反应
B.慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C.慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D.恒温恒容时,充入惰性气体,压强增大,平衡向右移动,混合气体的颜色变浅
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子分子。
试回答下列问题:
(1)写出A、B、E元素的名称:A________;B________;E________。
(2)C元素的原子的电子式为________,D元素的原子结构示意图为________,C与E形成的化合物的结构式为________。
(3)写出下列物质的电子式:
A2B2________________;E2B2_______________;
A2C________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学校课外活动小组仅有一大一小两试管和氢氧化钠溶液。甲、乙两个同学找来铝制废牙膏皮,各自设计了一套装置如下图,制取并收集一试管氢气。
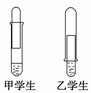
(1)哪个学生设计的装置比较合理?____(填“甲”或“乙”),另一设计装置不合理的原
因________________________________________________________________________
________________________________________________________________________。
(2)用比较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是
________________________________________________________________________。
(3)还可以用哪些常见物品和试剂代替废牙膏皮和氢氧化钠溶液完成实验?
________________________________________________________________________
________________________________________________________________________。
(4)测定H2和空气混合气体的爆炸范围实验如下所述。取10支大试管,依次盛水90%(体积分数)、80%……再用排水集气法收集H2,而后分别把试管口移近酒精灯火焰,实验结果如下:
| H2体积分数/% | 90 | 80 | 70 | 60~20 | 10 | 5 |
| 空气体积分数/% | 10 | 20 | 30 | 40~80 | 90 | 95 |
| 点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱爆炸 | 强爆炸 | 弱爆炸 | 不燃烧 不爆炸 |
由上述实验结果评价:用向下排空气法收集H2,保持试管倒置移近火焰,如果只发出轻微的“噗声”,表示收集的H2已纯净的说法的真正涵义:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作叙述正确的是( )
A.萃取操作必须在分液漏斗中进行
B.振荡试管中液体时,手拿住试管,用手腕甩动
C.用剩的药品应收集起来,放回原试剂瓶中
D.称量物质时,先取小砝码,再依次取较大的砝码
查看答案和解析>>
科目:高中化学 来源: 题型:
下列是常用的中和胃酸的药物:
| 药名 | 小苏打 | 胃舒平 | 达喜 |
| 化学式 | NaHCO3 | Al(OH)3 | Al2Mg6(OH)16CO3·4H2O |
| 每片药量 | 0.50 g | 0.245 g | 0.5 g |
(1)胃舒平的摩尔质量是________。
(2)估算10片胃舒平和5片达喜,含铝的物质的量较多的是________。
(3)某瓶小苏打有100粒药片,则该瓶药含小苏打的物质的量为________(保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2,发生如下反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。2 min后,反应达到平衡,生成SO3为1.4 mol,同时放出热量Q kJ。则下列分析正确的是 ( )。
A.在该条件下,反应前后的压强之比为6∶5.3
B.若反应开始时容器体积为2 L,则v(SO3)=0.35 mol/(L·min)
C.若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)<1.4 mol
D.若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量大于
Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z为同一短周期中的元素,其原子半径依次减小,它们的最高价氧化物对应水化物之间,任意两种混合均可反应,M为Y、Z形成的化合物,其溶液显酸性。下列说法正确的是( )
A.其简单离子的半径依次增大
B.将M溶液加热蒸干并灼烧,最后可得Y的氧化物
C.X燃烧的产物中只含离子键
D.将少量X单质投入到M溶液中,会置换出Y单质
查看答案和解析>>
科目:高中化学 来源: 题型:
将总物质的量为n mol的钠和铝的混合物(其中钠的物质的量分数为x),投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V L。下列关系式中正确的是( )
A.x=V/(11.2n) B.0<x≤0.5 C.V=33.6n(1-x) D.11.2n<V≤22.4n
查看答案和解析>>
科目:高中化学 来源: 题型:
已知31 g白磷变成红磷放出18.39 kJ热量,下列两反应中:
①P4(s,白)+5O2(g)===2P2O5(s) ΔH=Q1 kJ·mol-1
②4P(s,红)+5O2(g)===2P2O5(s) ΔH=Q2 kJ·mol-1
则下列说法正确的是( )
A.Q1>Q2,白磷比红磷稳定
B.Q1>Q2,红磷比白磷稳定
C.Q1<Q2,白磷比红磷稳定
D.Q1<Q2,红磷比白磷稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com