
| A. | Mg、Al | B. | Se,Br | C. | Si、Ge | D. | S、As |
科目:高中化学 来源: 题型:选择题
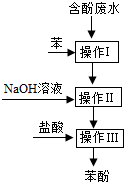
| A. | 操作I中苯作萃取剂 | |
| B. | 苯酚钠在苯中的溶解度比在水中的大 | |
| C. | 通过操作II苯可循环使用 | |
| D. | 三步操作均需要分液漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯(乙炔):将气体通过盛KMnO4溶液的洗气瓶 | |
| B. | 溴乙烷(溴):加入CCl4,振荡,静置,分液 | |
| C. | 苯(苯酚):加足量NaOH溶液,振荡,静置,分液 | |
| D. | 乙醛(乙酸乙酯):加入NaOH溶液,振荡,静置,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 由Cu、Zn、稀H2S04形成如下图甲、乙装置.试回答以下问題:
由Cu、Zn、稀H2S04形成如下图甲、乙装置.试回答以下问題:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图所示装置检验对应气体时,不能达到目的是( )
用如图所示装置检验对应气体时,不能达到目的是( ) | 生成的气体 | 试剂X | 试剂Y | |
| A | 电石与水反应制取的乙炔 | CuSO4 | Br2的CCl4溶液 |
| B | 证明苯与液溴的反应是取代反应而不是加成反应 | 水 | AgNO3溶液 |
| C | CH3CH2Br与NaOH乙醇溶液共热制取的乙烯 | 水 | KMnO4酸性溶液 |
| D | C2H5OH与浓硫酸加热至170℃制取乙烯 | NaOH溶液 | Br2的CCl4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和Mg分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | 硅酸钠溶液通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| C. | F2与Cl2分别于足量的H2反应,判断氟和氯的非金属性强弱 | |
| D. | 在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,属于共价(“离子”或“共价”)化合物.
,属于共价(“离子”或“共价”)化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4的电极为正极 | |
| B. | 正极的电极反应式为:202+8e-+4H20=80H- | |
| C. | 若甲烷通人量为1.12L(标准状况)且反应完全,则电池中有0.1mol02被氧化 | |
| D. | 通入甲烷的电极的电极反应式为:CH4+202+4e-=C02+2H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
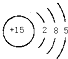 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com