


| 54 |
| 12 |
 ,F为
,F为 ,G为
,G为 ,B为
,B为 ,据此解答.
,据此解答.| 54 |
| 12 |
 ,F为
,F为 ,G为
,G为 ,B为
,B为 ,
, 发生消去反应生成
发生消去反应生成 ,反应④是
,反应④是 发生加成反应生成
发生加成反应生成 ,故答案为:消去反应;加成反应;
,故答案为:消去反应;加成反应;| △ |
| △ |
 )有很多同分异构体,满足以下条件的B的同分异构体:a.分子中有苯环 b.分子中有羧基,c.苯坏上有三个取代基,取代基为-COOH、2个-CH3,若2个-CH3相邻,-COOH有2种位置,若2个-CH3相间,-COOH有3种位置,若2个-CH3相对,-COOH有1种位置,符合条件的同分异构体共有2+3+1=6种,故答案为:6.
)有很多同分异构体,满足以下条件的B的同分异构体:a.分子中有苯环 b.分子中有羧基,c.苯坏上有三个取代基,取代基为-COOH、2个-CH3,若2个-CH3相邻,-COOH有2种位置,若2个-CH3相间,-COOH有3种位置,若2个-CH3相对,-COOH有1种位置,符合条件的同分异构体共有2+3+1=6种,故答案为:6.


科目:高中化学 来源: 题型:
| A、目前用量最大的合金是铝合金 |
| B、氧化镁用作耐火材料 |
| C、有机玻璃不是玻璃,是塑料 |
| D、钢化玻璃不是合金,是玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:

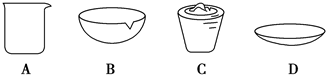
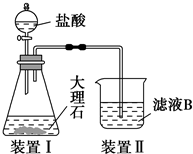
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl-CO32- NO3- SO42- SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
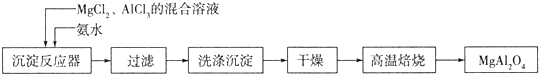
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 )
)| 实验序号 | 混合物 质量 | 物质的量关系n(Y)/n(Z) | 产物的量 | ||
| m(CO2)/g | m(H2O)/g | V(N2)/mL | |||
| ① | 3g | 2:3 | 3.08 | 1.8 | 672 |
| ② | 3g | 3:2 | 3.52 | 1.8 | 448 |
查看答案和解析>>
科目:高中化学 来源: 题型:
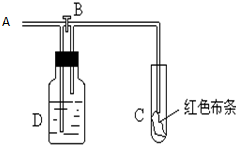 如图:A处通入氯气.关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色.由此作出的判断正确的是( )
如图:A处通入氯气.关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色.由此作出的判断正确的是( )| A、D中可能是浓硫酸 |
| B、通入的氯气含有水蒸气 |
| C、D中可能是水 |
| D、D中不可能是NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com