
| A. | CuO溶于稀H2SO4 | B. | NaOH溶液和HNO3溶液反应 | ||
| C. | KOH溶液和CH3COOH溶液反应 | D. | Ba(OH)2 溶液和H2SO4溶液反应 |
分析 离子方程式H++OH-=H2O表示强酸和强碱反应生成可溶性的盐和水的一类化学反应,据此对各选项进行判断.
解答 解:A.氧化铜是碱性氧化物,离子方程式中不能拆开,反应的离子方程式为:CuO+2H+═H2O+Cu2+,不能用H++OH-=H2O来表示,故A错误;
B.氢NaOH是强碱,硝酸是强酸,硝酸钠是可溶于水的盐,所以NaOH和HNO3溶液的反应能用H++OH-=H2O来表示,故B正确;
C.醋酸是弱酸,CH3COOH+KOH反应的离子反应为:CH3COOH+OH-=CH2COO-+H2O,不能用“H++OH-═H2O”表示,故C错误;
D.H2SO4与Ba(OH)2反应的离子反应为:2H++2OH-+Ba2++SO42-=BaSO4↓+2H2O,不能用“H++OH-═H2O”表示,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,明确离子方程式表示的意义为解答关键,注意掌握离子方程式的书写原则,试题培养了学生的规范答题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在一块镀锡铁板刻一划痕,滴加酸化的食盐水浸泡及KSCN溶液,溶液颜色没有变化,判断其具有好的耐腐蚀性 | |
| B. | 测定一定物质的量浓度的某NaA溶液的pH,pH>7,可以说明HA是弱酸 | |
| C. | 在氯化银的悬浊液中加入碘化钠溶液,沉淀颜色不变,说明氯化银的溶解度比碘化银大 | |
| D. | 在酸碱中和滴定中,用标准氢氧化钠溶液测定醋酸溶液的浓度时,用甲基橙做指示剂对滴定终点的判断比用酚酞的更准确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
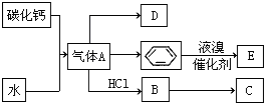 已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空:
已知:C是一种合成树脂,用于制备塑料和合成纤维,D是一种植物生长调节剂,用它可以催熟果实.根据以下化学反应框图填空: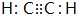 ;C的结构简式
;C的结构简式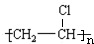 ;
; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr;其反应类型为取代反应.
+HBr;其反应类型为取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 维生素C用作贫血患者补铁剂的搭档 | |
| B. | 生石灰用作煤炭燃烧的固硫剂 | |
| C. | 氯化铁溶液用于腐蚀印刷电路板 | |
| D. | 高铁酸盐(Na2FeO4)用于饮用水的处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用丁达尔效应可区分溶液和胶体 | |
| B. | 能使湿润的监色石蕊试纸变红的气体是NH3 | |
| C. | 观察钾元素的焰色反应时要透过监色钴玻璃 | |
| D. | 检验溶液中SO42-存在时,先加盐酸酸化,再加氯化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com