
| A.16 | B.9 | C.15 | D.7 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.用溶解度数据判断煮沸Mg (HCO3)2溶液得到的产物是Mg(OH)2而不是 MgCO3 |
| B.用沸点数据推测将一些液体混合物用分馏的方法分离开来的可能性 |
| C.利用溶液的pH与7的大小关系,来判断任何温度下溶液的酸碱性 |
| D.用原子(或离子)半径数据推断某些原子(或离子)氧化性或还原性的强弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.②④ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若X、Y原子序数相差1,Y为ⅡA族,则X一定是ⅢA族 |
| B.若H n XO m为强酸,则X的氢化物溶液于水一定显酸性 |
| C.若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
| D.若Y(OH)m易溶于水,则X(OH)n一定不溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
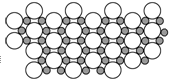
| A.MgB | B.MgB2 | C.Mg2B | D.MgB6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶体中分子间作用力越大,分子越稳定 |
| B.乙醇的沸点比甲醚(CH3—O—CH3)高,主要原因是乙醇分子间能形成氢键 |
| C.红宝石、蓝宝石和金刚石都是由碳元素组成的宝石 |
| D.非金属的最高价含氧酸都具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | M | F | |
| 电离能(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
| | 熔点/K | 沸点/K | 标准状况时在水中的溶解度 |
| H2S | 187 | 202 | 2.6 |
| H2C2 | 272 | 423 | 比任意比互溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com