
【题目】下列五种有机物中:A.CH4;B.CH2=CH2;C.CH3CH2OH;D.CH3COOH;E.淀粉。
(1)C分子中含有的官能团的名称是_____;
(2)A分子的结构式是_____;
(3)水溶液显酸性的是_____(填编号);
(4)可用于合成聚乙烯塑料的是_____(填编号),化学反应方程式为_____________________ ;
(5)通常用于检验碘单质的是_____(填编号)。
【答案】羟基 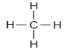 D B nCH2 = CH2→
D B nCH2 = CH2→![]() E
E
【解析】
(1)醇的官能团是羟基;
(2) CH4分子中4个H原子通过4个单键与C原子结合;
(3)羧酸能电离出氢离子,具有酸性;
(4)乙烯发生加聚反应生成聚乙烯;
(5)碘单质能使淀粉变蓝。
(1) CH3CH2OH是乙醇,分子中含有的官能团的名称是羟基;
(2) CH4分子中4个H原子通过4个单键与C原子结合,CH4分子的结构式是 ;
;
(3) CH3COOH能电离出氢离子,具有酸性,水溶液显酸性的是CH3COOH,选D;
(4)乙烯发生加聚反应生成聚乙烯;可用于合成聚乙烯塑料的是CH2=CH2,选B;化学反应方程式为nCH2 = CH2→![]() ;
;
(5) 碘能使淀粉变蓝,通常用于检验碘单质的是淀粉,选E。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在2 L恒容密闭容器中,800 ℃时反应2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)图中表示NO2的变化的曲线是________。
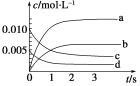
(2)能说明该反应已经达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v(NO)逆=2v(O2)正
d.容器内的密度保持不变
(3)能够使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体
b.增大O2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国最新战机歼-31使用了高强度、耐高温的钛合金材料。工业上冶炼钛的反应:TiCl4+2Mg==Ti+2MgCl2,下列有关该反应的说法正确的是()

A. TiCl4是还原剂
B. Mg得到电子
C. TiCl4发生氧化反应
D. Mg被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:P4(g)+6Cl2(g)===4PCl3(g) ΔH=a kJ·mol-1,
P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1,
又知形成或拆开1 mol化学键放出或吸收的能量称为该化学键的键能。P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ·mol-1,PCl3中P-Cl键的键能为1.2c kJ·mol-1。下列叙述正确的是
A. P-P键的键能大于P-Cl键的键能
B. 可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C. Cl-Cl键的键能为(b-a+5.6c)/4 kJ·mol-1
D. P-P键的键能为(5a-3b+12c)/8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 3.6 g 碳在 6.4 g 的氧气中燃烧,至反应物耗尽,并放出 X kJ 热量。已知单质 C(s)的燃烧热数值为 Y kJ·mol-1,则 1 mol C(s)与 O2(g)反应生成 CO(g)的反应热 ΔH 为( )
A. -Y kJ/mol B. -(10X-Y) kJ/mol C. -(5X-0.5Y) kJ/mol D. +(10X-Y) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应,前后均可以用同一个离子方程式表示的是
A.HCl+Na2CO3 HCl+NaHCO3
B.HCl+Na2CO3 H2SO4+K2CO3
C.H2S+NaOH H2SO4+KOH
D.BaCl2+Na2SO4 BaCO3+H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在1L恒容密闭容器中加入lmol的N2(g)和3molH2(g)发生反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确的是( )
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确的是( )
时间(min) | 0 | t1 | t2 | t3 |
NH3物质的量(mol) | 0 | 0.2 | 0.3 | 0.3 |
A. 0t1min,v(NH3)=0.2/t1mol·L-1·min-1
B. t3时再加入1mol的N2(g)和3molH2(g),反应达新平衡时,c(N2)>0.85mol·L-1
C. N2(g)+3H2(g) ![]() 2NH3(g)的活化能小于2NH3(g)
2NH3(g)的活化能小于2NH3(g) ![]() N2(g)+3H2(g)的活化能
N2(g)+3H2(g)的活化能
D. 升高温度,可使正反应速率减小,逆反应速率增大,故平衡逆移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com