
【题目】某同学查阅资料获悉:用KMnO4可以测定H2O2的物质的量浓度:取15.00mL H2O2溶液,用稀H2SO4酸化;逐滴加入0.003mol·L-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至恰好完全反应时共消耗20.00 mL KMnO4溶液。该反应的离子方程式是:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;
(1)该反应体现了H2O2的__________(填“氧化性”、“还原性”或“氧化性和还原性”);
(2)KMnO4溶液褪色速率开始较慢,后变快的原因可能是某种物质对该反应起到了催化作用,则该物质最有可能是________;(填序号) a. MnO4- b.H+ c.Mn2+ d.K+
(3)判断完全反应的现象是_________________________________________________;
(4)该H2O2溶液的物质的量浓度是__________________。
【答案】 还原性 c 当加入最后一滴KMnO4溶液时,溶液变为红色 0.01 mol·L-1
【解析】(1)H2O2中O元素的化合价从-1价升高到了O2中O元素的0价,所以H2O2作还原剂,体现了还原性。
(2)由离子方程式可知,反应后生成了Mn2+,开始Mn2+浓度较小,反应速率慢,反应一段时间后,Mn2+浓度变大,反应速率加快,故起催化作用的物质是Mn2+
(3)KMnO4溶液显紫色,当KMnO4溶液与H2O2发生氧化还原反应时,溶液无色,当H2O2完全反应后,再滴入一滴KMnO4溶液,溶液将由无色变为红色,此时就是滴定的终点。故答案为:当加入最后一滴KMnO4溶液时,溶液变为红色 。
(4)消耗的KMnO4的物质的量为0.02L×0.003mol·L-1=6×10-5mol,根据方程式可知H2O2的物质的量为![]() ×6×10-5mol=1.5×10-4mol,所以H2O2溶液的物质的量浓度c=1.5×10-4mol÷0.015L = 0.01 mol·L-1
×6×10-5mol=1.5×10-4mol,所以H2O2溶液的物质的量浓度c=1.5×10-4mol÷0.015L = 0.01 mol·L-1


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1moI/L的是
A. 将6.2gNa2O溶解于水,并配成200mL溶液
B. 1L含1mol K+的K2SO4溶液
C. 将22.4LHC1溶于1L水
D. 将40.0 g NaOH溶于1L水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
A. NaOH(固体) B. 同浓度盐酸 C. NaCl(固体) D. CH3COONa(固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO(NH2) 2(尿素)在工业生产中可用于制氢、脱硫脱硝等。回答下列问题:
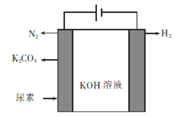
(1)用惰性电极电解尿素制氢的装置如图所示。
①应将尿素加入该电解池的________(填“阳极”或“阴极”)。
②阴极的电极反应式为________。
③当生成1 mol H2时,消耗尿素________g。
(2)尿素/次氯酸钙溶液可用于脱硫脱硝。
①若脱硝时,尿素将等物质的量的N0和N02转化为N (次氯酸钙作催化剂),则 n(N0): n(N02):C0(NH2)2]=________。
②向尿素/次氯酸钙溶液中加入熟石灰可提高脱硫脱硝率,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期元素,非金属元素A的最外层电子数与其周期数相等,B的成对电子与未成对电子所占据的原子轨道数相等。单质B在单质C中充分燃烧生成BC2。 D+与C2-具有相同的电子数。A在E中燃烧,产物溶于水会得到一种强酸。
(1)B在元素周期表中的位置是________,写出一种工业制备单质E的化学方程式:_____。
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为________,其阴离子中B原子的杂化方式为__________。
(3)由这些元素组成的某些物质的组成和结构信息如下表:
物质 | 组成和结构 |
a | A、D两元素组成的离子化合物 |
b | 由C、D两元素组成的含有非极性键的离子化合物 |
c | 化学组成为BCE2 |
a的电子式为_________;b的化学式为________;c的空间构型为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是物质的量概念及其相关计算的内容,完成相关填空:
(1)标准状况下,① 4 g氢气、②33.6 L甲烷、③6.02×1023个水分子中,含分子数最多的是(填序号,下同)_______,含原子数最多的是_________,质量最大的是___________,体积最小的是___________。
(2)在标准状况下,1L的密闭容器中恰好可盛放n个N2分子和m个H2分子组成的混合气体,则阿伏加德罗常数可表示为___________。
(3)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,A的相对原子质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。已知一种合成阿魏酸的反应可表为:
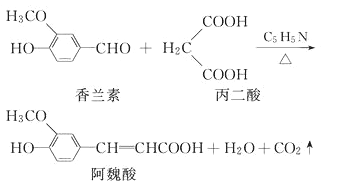
对以上反应说法正确的是
A. 可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与Na2CO3、NaOH 、NaHCO3溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体分子中有4种不同化学环境的氢,能消2molNaOH溶液且能发生银镜反应的酚类化合物共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 电解熔融氯化镁可制取金属镁
B. 电解饱和食盐水可制取氯气
C. 生产普通玻璃的主要原料为石灰石、纯碱和晶体硅
D. 接触法制硫酸的硫元素主要来源于硫黄或含硫矿石
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com