
| A. | 丙烯分子里碳氢原子的个数比为1:2 | |
| B. | 丙烯完全燃烧生成的CO2和H2O的物质的量相等 | |
| C. | 丙烯能使酸性KMnO4溶液褪色 | |
| D. | 丙烯易与溴水发生加成反应,且1 mol乙烯完全加成需消耗1 mol溴单质 |
分析 丙烯分子式为C3H6,与环丙烷互为同分异构体,如含有碳碳双键,可与溴水发生加成反应,可通过消耗的溴的量的关系判断是否含有碳碳双键,如含有碳碳双键,可发生加成反应和氧化反应,以此解答该题.
解答 解:A.分子里碳、氢原子个数比为1:2不能说明含有碳碳双键,如环丙烷,故A错误;
B.丙烯完全燃烧生成的CO2和H2O的物质的量相等只能说明其碳、氢原子个数之比,不能说明含有碳碳双键,故B错误;
C.能使酸性高锰酸钾溶液褪色的不一定是碳碳双键,碳碳三键也能使酸性高锰酸钾溶液褪色,故C错误;
D.丙烯与溴发生加成反应时,丙烯和溴的物质的量之比等于反应的计量数之比,所以能证明含有一个碳碳双键,故D正确.
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握实验证明的角度和合理性的评价,难度不大.


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案科目:高中化学 来源: 题型:解答题
 已知A、B、C、D是中学化学中常见的四种不同微粒.它们之间存在如图中转化关系:
已知A、B、C、D是中学化学中常见的四种不同微粒.它们之间存在如图中转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子交换法可以软化硬水 | |
| B. | 生产、生活使用的天然水必须经软化 | |
| C. | 硬水中含有较多Ca2+、Mg2+ | |
| D. | 加热可使暂时硬水中的Ca2+生成CaCO3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用聚乳酸塑料代替聚乙烯塑料可减少白色污染 | |
| B. | 煤油、“乙醇汽油”、“生物柴油”都是碳氢化合物 | |
| C. | 为防治碘缺乏病,在食用盐中添加适量的碘酸钾 | |
| D. | 甘油可用作护肤保湿剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液、水 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 除去CH4中的C2H4 | ]试管、带导管的橡皮塞 | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 路线①②③是工业生产硝酸的主要途径 | |
| B. | 路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 | |
| C. | 上述所有反应都是氧化还原反应 | |
| D. | 上述反应中①②③均属于氮的固定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定元素种类的是--电子数 | |
| B. | 决定元素化学性质的是--原子的核外电子数 | |
| C. | 决定元素相对原子质量的是--中子数 | |
| D. | 决定元素周期表中原子序数的是--核电荷数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
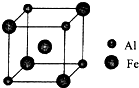 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com