
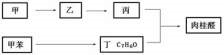
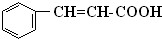 ,与甲醇反应得到肉桂酸甲酯;
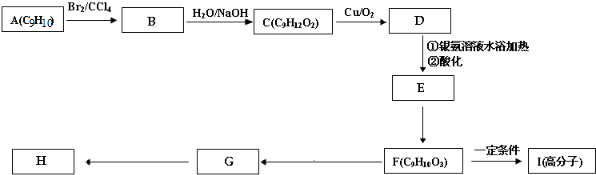
,与甲醇反应得到肉桂酸甲酯;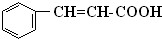 ,G与F的分子式可知,应是F发生消去反应脱去1分子水生成G,芳香烃A的分子式为C9H10,饱和度为
,G与F的分子式可知,应是F发生消去反应脱去1分子水生成G,芳香烃A的分子式为C9H10,饱和度为| 2×9+2-10 |
| 2 |
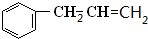 ,A与溴发生加成反应生成B为
,A与溴发生加成反应生成B为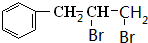 ,B发生水解反应生成C为
,B发生水解反应生成C为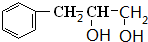 ,C发生催化氧化生成D为
,C发生催化氧化生成D为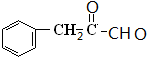 ,D与银氨溶液反应、酸化得到F为
,D与银氨溶液反应、酸化得到F为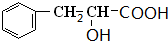 ,F发生缩聚反应生成高分子化合物I为
,F发生缩聚反应生成高分子化合物I为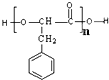 ,据此解答.
,据此解答.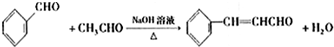 ,
,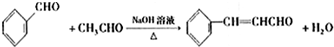 ;
;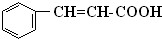 ,与甲醇反应得到肉桂酸甲酯,肉桂酸甲酯的结构简式为:
,与甲醇反应得到肉桂酸甲酯,肉桂酸甲酯的结构简式为: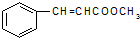 ,
,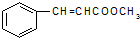 ;
;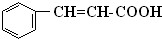 ,G与F的分子式可知,应是F发生消去反应脱去1分子水生成G,芳香烃A的分子式为C9H10,饱和度为
,G与F的分子式可知,应是F发生消去反应脱去1分子水生成G,芳香烃A的分子式为C9H10,饱和度为| 2×9+2-10 |
| 2 |
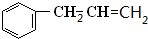 ,A与溴发生加成反应生成B为
,A与溴发生加成反应生成B为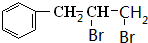 ,B发生水解反应生成C为
,B发生水解反应生成C为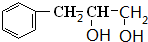 ,C发生催化氧化生成D为
,C发生催化氧化生成D为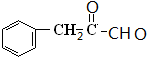 ,D与银氨溶液反应、酸化得到F为
,D与银氨溶液反应、酸化得到F为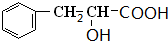 ,F发生缩聚反应生成高分子化合物I为
,F发生缩聚反应生成高分子化合物I为 ,
,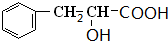 ,F→G发生醇的消去反应,
,F→G发生醇的消去反应,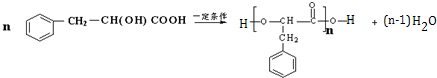 ;
; ,
,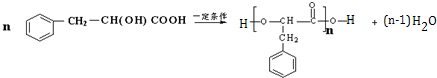 ;
; ;
;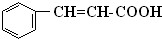 )的同分异构体中,属于酯类且苯环上只有一个取代基的同分异构体有
)的同分异构体中,属于酯类且苯环上只有一个取代基的同分异构体有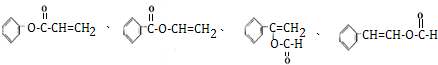 ,
,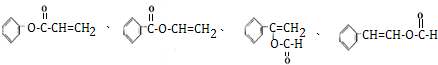 .
.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
 某兴趣小组利用如图所示装置进行实验,对钢铁的电化学腐蚀原理进行探究.
某兴趣小组利用如图所示装置进行实验,对钢铁的电化学腐蚀原理进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③⑦ | B、②④⑥ |
| C、②④⑤ | D、②⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
135 53 |
135 53 |
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石(Na3AlF6)的化学方程式为:2Al(OH)3+12HF+3A=2Na3AlF6+3CO2↑+9H2O
冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石(Na3AlF6)的化学方程式为:2Al(OH)3+12HF+3A=2Na3AlF6+3CO2↑+9H2O查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在由水电离出的C(H+)=10-13 mol?L-1的溶液中:NH4+、Na+、Cl-、AlO2- |
| B、在强碱性溶液中:Na+、K+、CO32-、NO3- |
| C、在pH=12的溶液中:NH4+、Na+、SO42-、Cl- |
| D、在C(H+)=0.1 mol?L-1的溶液中:K+、I-、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com