
| A. | 用惰性电极电解含酚酞的饱和食盐水,阳极附近溶液先变红 | |
| B. | 铜的电解精炼过程中,有0.2 mol 电子发生转移时,阳极一定有6.4 g铜溶解 | |
| C. | 将地下钢管与直流电源的正极相连,称为外加电源的阴极保护法 | |
| D. | 在中性环境中,每生成35.6 g铁锈(Fe2O3•H2O),消耗的氧气为6.72 L(标准状况) |
分析 A、电解饱和食盐水时,阳极氯离子放电生成氯气,不会生成氢氧化钠;
B、在电解精炼铜时,阳极上是粗铜,放电的不只是铜,还有比铜活泼的金属杂质;
C、将地下钢管与直流电源的正极相连,则钢管作为阳极,会被腐蚀;
D、根据反应O2+2H2O+4e-=4OH-,结合铁元素守恒可得关系式$\frac{3}{2}$O2~2Fe(OH)3~Fe2O3.H2O计算.
解答 A、用惰性电极电解饱和食盐水时,阳极生成氯气,阴极生成氢气和氢氧根离子,所以阴极生成氢氧化钠,阴极附近溶液先变红,故A错误;
B、在电解精炼铜时,阳极上是粗铜,故阳极上放电的不只是铜,还有比铜活泼的金属杂质,故当转移0.2 mol 电子转移时,阳极上溶解的质量小于6.4,故B错误;
C、将地下钢管与直流电源的正极相连,则钢管作为阳极,会被腐蚀,故C错误;
D、根据反应O2+2H2O+4e-=4OH-,结合铁元素守恒可得关系式$\frac{3}{2}$O2~2Fe(OH)3~Fe2O3.H2O,35.6g铁锈(Fe2O3•H2O)的物质的量为0.2mol,故消耗氧气0.3mol,标况下的体积为0.3×22.4=6.72L,故D正确;
故选D.
点评 本题考查了电解饱和食盐水的原理、阿伏伽德罗常数及氧化还原的有关计算,掌握原理和相关计算公式是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
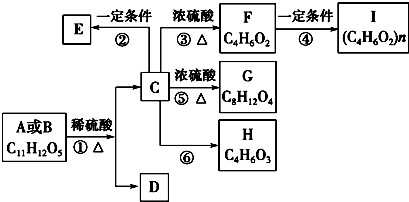
 .
.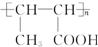
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
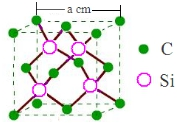 物质结构与性质包括原子、分子和晶体结构与性质三大内容.请回答下列问题:
物质结构与性质包括原子、分子和晶体结构与性质三大内容.请回答下列问题: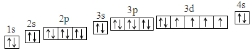 ;第ⅦA族元素原子外围电子排布通式为ns2np5.
;第ⅦA族元素原子外围电子排布通式为ns2np5.| H | B | C | N | O | F |
| 2.18 | 2.04 | 2.55 | 3.04 | 3.44 | 3.98 |
| Si | P | S | Cl | ||
| 1.90 | 2.19 | 2.58 | 3.16 |
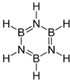 ,能发生加成反应、取代反应(填有机反应类型).
,能发生加成反应、取代反应(填有机反应类型).| 氨 | 三氟化氮 | |
VSEPR模 型 | 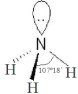 | 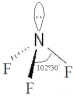 |
| 熔点/℃ | -77.7 | -206.8 |
| 沸点/℃ | -33.5 | -129.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
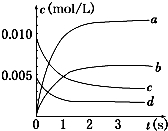 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
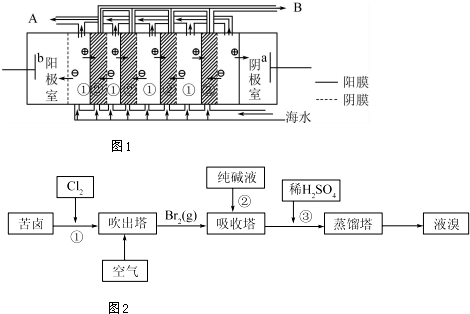
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 氢键X-H…Y | 键能kJ.mol-1 |
| (HF)n | D-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.| 序号 |  | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
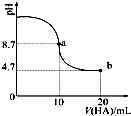 室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )| A. | a点所示溶液中c(HA)>c(A-) | |
| B. | 当加入HA溶液10ml时,$\frac{{K}_{W}}{c({H}^{+})}$<1.0×10-7mol•L-1 | |
| C. | a点所示溶液中c(Na+)=c(A-)+c(HA) | |
| D. | b点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com