
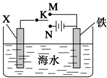
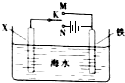
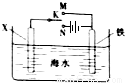
 利用如图装置可以模拟铁的电化学防护.下列说法不正确的是( )
利用如图装置可以模拟铁的电化学防护.下列说法不正确的是( )

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
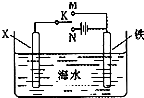 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是查看答案和解析>>
科目:高中化学 来源: 题型:
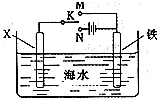 铁、铝是现代金属材料的主角.
铁、铝是现代金属材料的主角.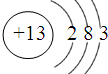

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀 |
| B.若X为锌棒,开关K置于M处,铁极发生氧化反应 |
| C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀 |
| D.若X为碳棒,开关K置于N处,X极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京四中高二(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com