
科目:高中化学 来源:2014-2015山西省原平市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子方程式的书写正确的是
A.铁和稀硫酸反应:2Fe + 6H+ =2Fe 3+ +3H 2↑
B.纯碱溶液中通入二氧化碳:CO32―+ CO2 + H2O = 2HCO3―
C.钠和冷水反应 Na+2H2O = Na++2OH+H2↑
D.氯化铝溶液中加入过量的氨水 Al3+ + 4NH3·H2O = AlO2- + 4NH4++ 2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015山西省原平市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知反应3A(g)+B(g) C(s)+4D(g)+Q,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是
C(s)+4D(g)+Q,下图中a、b表示一定条件下,D的体积分数随时间t的变化情况。若要使曲线b变为曲线a,可采取的措施是

①增大B的浓度 ②升高反应温度
③缩小反应容器的体积(加压) ④加入催化剂
A.①② B.①③ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列事实不能证明HNO2是弱电解质的是
①c(H+)=0.1molL﹣1的HNO2溶液稀释至1000倍,pH<4
②用HNO2溶液做导电实验,灯泡很暗
③等pH、等体积的盐酸和HNO2溶液中和碱时,HNO2的中和碱能力强
④0.1molL﹣1HNO2溶液的pH=2
⑤HNO2与CaCO3反应放出CO2气体.
A.①⑤ B.②⑤ C.③⑤ D.③④
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列各组离子,能在溶液中大量共存的是
A.Na+、Al3+、AlO2-、Br- B.H+、Fe2+、SO42-、NO3-
C.K+、NH4+、CO32-、OH- D.Ca2+、Al3+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南七校高一上学期期末联考化学试卷(解析版) 题型:实验题
(13分)实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_____ 。
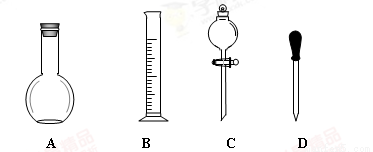
(2)在容量瓶的使用方法中,下列操作不正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取的质量为 g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度 0.1mol/L(填“大于”“小于”或“等于”)。
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为 mL,如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南七校高一上学期期末联考化学试卷(解析版) 题型:选择题
在无色透明的溶液中,能够大量共存的离子组是
A.Al3+、Ca2+、Cl -、NO3- B.Ba2+、K+、CO32-、Cl -
C.Na+、Cu2+、NO3-、HCO3- D.Na+、Fe2+、Cl -、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市八校高三3月联考理综化学试卷(解析版) 题型:选择题
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.醋酸的电离程度增大,c(H+)亦增大
C.溶液中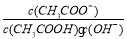 不变
不变
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:实验题
(本题共12分)工业烧碱成分NaOH、Na2CO3和可溶于水但不与酸反应的杂质,工业纯碱成分Na2CO3、NaHCO3和可溶于水但不与酸碱反应的杂质。为测定碱中各成分的百分含量可采用滴定法、气体法等。
完成下列填空:
(1)滴定法测定工业烧碱样品:配制250mL待测液,所用的主要仪器有烧杯、量筒、胶头滴管、玻璃棒、 。
(2)测定工业烧碱的总碱量n Na2O(或总耗酸量):进行滴定时,先向盛待测液的锥形瓶中加 作为指示剂。
判断滴定终点的现象是 。
(3)气体法测定工业烧碱的Na2CO3含量(如图):
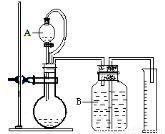
装置中B部分盛放的试液是 。
装置中A部分的分液漏斗与烧瓶之间连接的导管所起的作用是 。
(4)用中和滴定的氯化钡法测定工业烧碱中NaOH的含量时,可先在混合液中滴加过量的BaCl2溶液,再以酚酞作指示剂,然后用标准盐酸滴定。
滴加过量的BaCl2溶液目的是 。
向混有碳酸钡沉淀的氢氧化钠溶液中滴入盐酸,为什么不会使碳酸钡溶解而能测定氢氧化钠的含量 。
(5)用中和滴定的氯化钡法测定工业纯碱中NaHCO3的含量时,使用与测定烧碱相同的实验操作,过程稍作改变即可。
简述该操作过程 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com