
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向浑浊的苯酚试液中加入饱和Na2CO3溶液 | 溶液变澄清 | 酸性:苯酚>碳酸 |
| B | AgCl沉淀中滴入Na2S溶液 | 白色沉淀变黑色 | Ag2S比AgCl更难溶 |
| C | 向AlCl3溶液中滴入适量NaOH溶液 | 产生白色沉淀 | Al(OH)3不溶于碱 |
| D | 用玻璃棒蘸取某溶液在酒精喷灯上灼烧 | 火焰呈黄色 | 说明该溶液中一定含钠元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 + 6HCHO = 3H++ 6H2O + (CH2)6N4H+
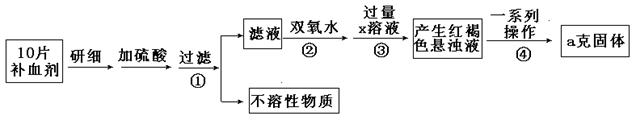
+ 6HCHO = 3H++ 6H2O + (CH2)6N4H+| 滴定次数 | 待测液的体积(mL) | 标准溶液的体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

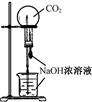
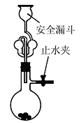
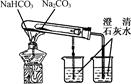
| A.测定一定时间内生,成H2的反应速率 | B.用CO2做,喷泉实验 | C.实验室制氢气 | D.比较Na2CO3与,NaHCO3的热稳定性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
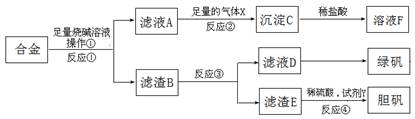
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com