
| A.利用太阳能蒸馏海水是海水淡化的方法之一 |
| B.研制乙醇汽油技术,可降低机动车辆尾气中有害气体的排放 |
| C.光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 |
| D.绿色化学的核心是利用化学原理从源头上减少和消除工农业生产等对环境的污染 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:计算题
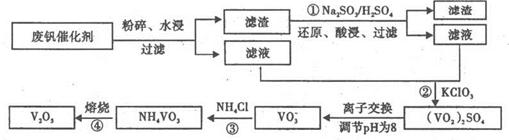

 VO2++V3++H2O
VO2++V3++H2O
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.他们的研究对人类的生命活动具有重要意义? |
| B.他们的研究有助于探索一些包括恶性肿瘤疾病的发生机理? |
| C.他们的研究深入到了细胞的层次? |
| D.他们的研究深入到了分子、原子的层次? |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.11.2L | B.33.6L | C.22.4L | D.44.8L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5 | B.6 | C.7 | D.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学是一门以实验为基础的自然科学 |
| B.化学是一门具有较强实用性的科学 |
| C.化学支持高新技术的快速发展,但面对伪科学和人体健康等问题却显得无能为力 |
| D.化学将为解决能源问题、环境问题、资源问题等提供有效途径和方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com