
在合成氨工业中,下列事实不能用勒沙特列原理解释的是
[ ]
A.向循环气体中不断补充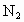 和
和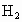 ,并将生成的
,并将生成的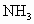 及时地从混合气体中分离出去,这样做有利于合成氨的反应
及时地从混合气体中分离出去,这样做有利于合成氨的反应
B.加入催化剂有利于合成氨的反应
C.高压有利于合成氨的反应
D.500℃左右比室温更有利于合成氨的反应
|
增大反应物浓度并减小生成物浓度,能使反应向生成氨的方向移动;合成氨反应的特点之一是正,反应是气体体积缩小的反应,当其他条件不变时,增大压强平衡向减小压强即向气体体积减少方向移动,所以高压将有利于氨的合成,选项 A、C能用勒沙特列原理解释.由于使用铁触媒能同等程度地加快正、逆反应速率,所以不破坏化学平衡状态,平衡不发生移动,只能缩短达到平衡的时间,合成  的另一特点是正反应为放热反应,低温虽有利于平衡向正反应方向移动,但反应速率太慢,生产周期太长,所以在生产上一般采用升高温度(500℃)加快反应速率的方法来提高 的另一特点是正反应为放热反应,低温虽有利于平衡向正反应方向移动,但反应速率太慢,生产周期太长,所以在生产上一般采用升高温度(500℃)加快反应速率的方法来提高 的生产率,选用500℃另一方面是考虑到催化剂活性最大,因此选项B、D不能用勒沙特列原理来解释. 的生产率,选用500℃另一方面是考虑到催化剂活性最大,因此选项B、D不能用勒沙特列原理来解释.
勒沙特列原理只能解释平衡移动问题,不能用于解释化学反应速率问题. |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
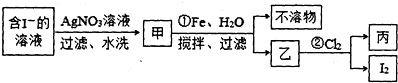
查看答案和解析>>
科目:高中化学 来源: 题型:021
在合成氨工业中,下列事实不能用勒沙特列原理解释的是
[ ]
A.向循环气体中不断补充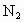 和
和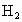 ,并将生成的
,并将生成的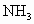 及时地从混合气体中分离出去,这样做有利于合成氨的反应
及时地从混合气体中分离出去,这样做有利于合成氨的反应
B.加入催化剂有利于合成氨的反应
C.高压有利于合成氨的反应
D.500℃左右比室温更有利于合成氨的反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com