
| A、离子键就是阴阳离子间的静电引力 |
| B、所有金属元素与所有非金属元素间都能形成离子键 |
| C、钠原子与氯原子结合成氯化钠后体系能量降低 |
| D、在离子化合物CaCl2中,两个氯离子间也存在离子键 |


科目:高中化学 来源: 题型:
| A、24.4g | B、25.5g |
| C、23.6g | D、24g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 化学反应 | 离子方程式 | 评价 |
| A | 碳酸钙与醋酸反应 | CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| B | 碳酸钠溶液中滴加过量的盐酸 | CO32-+2H+═CO2↑+H2O | 正确 |
| C | 石灰水中滴加少量KHCO3溶液 | HCO3-+Ca2++OH-═CaCO3↓+H2O | 错误,不满足Ca(OH)2的配比 |
| D | 硫酸氢钠溶液与足量氢氧化钡溶液混合 | 2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | 正确 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、K+、OH-、SO42- |
| B、Na+、Ba2+、OH-、SO42- |
| C、Na+、Mg2+、SO42-、OH- |
| D、Ca2+、SO42-、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4 | B、8 | C、16 | D、32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
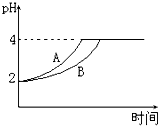 (1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是
(1)室温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com