
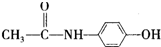
 ,从下简称F)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧、关节痛、神经痛、偏头痛等,它可用最简单的烯烃A等合成:
,从下简称F)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧、关节痛、神经痛、偏头痛等,它可用最简单的烯烃A等合成: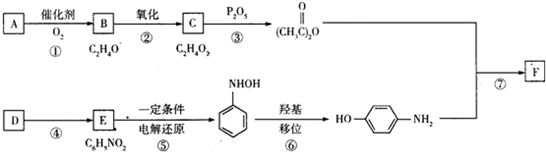
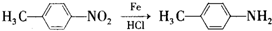
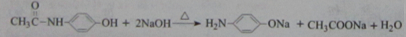 .
.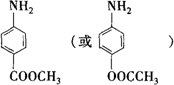 .
.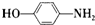 的合成路线
的合成路线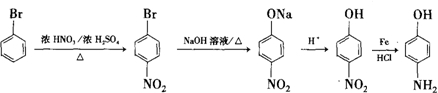 .
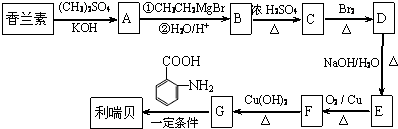
. 分析 根据题中各物质转化关系,A氧化得B,B氧化得C,根据B、C的分子式可知,A为CH3CH2OH,B为CH3CHO,C为CH3COOH,2分子C脱1分子水发生取代反应得乙酸酐,D在浓硫酸和浓硝酸的作用下生成硝基苯,所以D为苯,苯发生取代反应生成硝基苯,E还原得\重排得对氨基苯酚,与乙酸酐发生取代反应到F为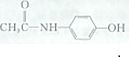 ,以此解答该题.
,以此解答该题.
解答 解:根据题中各物质转化关系,A氧化得B,B氧化得C,根据B、C的分子式可知,A为CH3CH2OH,B为CH3CHO,C为CH3COOH,2分子C脱1分子水发生取代反应得乙酸酐,D在浓硫酸和浓硝酸的作用下生成硝基苯,所以D为苯,苯发生取代反应生成硝基苯,E还原得\重排得对氨基苯酚,与乙酸酐发生取代反应到F为 ,
,
(1)由以上分析可知E为硝基苯,C为CH3COOH,含有的官能团为羧基,故答案为:硝基苯;羧基;
(2)反应④为苯发生取代反应生成硝基苯,故答案为:取代反应;
(3)由以上分析可知B为CH3CHO,故答案为:CH3CHO;
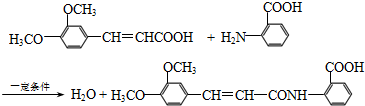
(4)F为 ,含有肽键和酚羟基,可与氢氧化钠溶液反应,方程式为
,含有肽键和酚羟基,可与氢氧化钠溶液反应,方程式为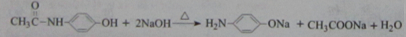 ,
,
故答案为: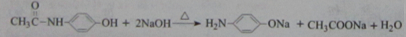 ;
;
(5)一类与E含有相同的官能团且与苯环直接相连,说明含有硝基,且与苯环直接相连,苯环的烃基有两种,当为乙基时有邻、间、对3种,当含有2个甲基时有6种同分异构体,共9种,另一类同分异构体同时满足下列条件:①属于对位二取代苯且苯环上连接一NH2;②能发生水解反应;③核磁共振氢谱有4组峰,则可能的结构有 ,
,
故答案为:9; ;
;
(6)需通过溴苯在对位引入羟基和氨基,首先溴苯发生硝化反应在对位引入硝基,然后水解生成酚羟基在还原生成氨基,对应的流程为 ,
,
故答案为: .
.
点评 本题考查有机物的推断和合成,为高频考点,把握合成流程这发生的反应、官能团的变化、有机物结构与性质为解答的关键,侧重分析与应用能力的考查,题目难度中等.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:解答题

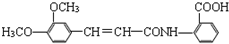 ).
).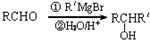
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
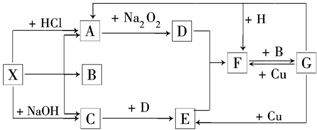
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N5+具有34个电子 | B. | N5+中氮-氮之间是以共价键结合 | ||
| C. | 化合物N5AsF6中As的化合价为+1 | D. | 化合物N5AsF6中F的化合价为-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀硫酸的反应 | |
| B. | 生石灰与水的反应 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知中和热为57.3kJ/mol,则HCl+NaOH═NaCl+H2O△H=-57.3kJ/mol | |
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)△H=+2×283.0kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. 同分异构体有4种.
同分异构体有4种. 的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例:
的合成路线(用流程图表示,无机试剂任选)注:合成路线的书写格式参照如下实例:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
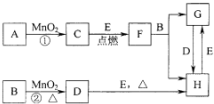 图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物.它们存在如下转化关系,反应中生成的水及次要产物均已略去.
图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物.它们存在如下转化关系,反应中生成的水及次要产物均已略去.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
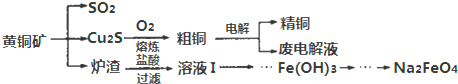
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com