
 Ä³Ń§ÉśĄūÓĆĻĀĆꏵŃé×°ÖĆĢ½¾æŃĪĒÅŹ½Ōµē³ŲµÄ¹¤×÷ŌĄķ£®°“ÕÕŹµŃé²½ÖčŅĄ“Ī»Ų“šĻĀĮŠĪŹĢā£ŗ
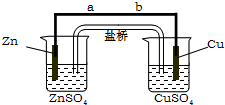
Ä³Ń§ÉśĄūÓĆĻĀĆꏵŃé×°ÖĆĢ½¾æŃĪĒÅŹ½Ōµē³ŲµÄ¹¤×÷ŌĄķ£®°“ÕÕŹµŃé²½ÖčŅĄ“Ī»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö £Ø1£©ZnĪŖøŗ¼«£¬CuĪŖÕż¼«£¬µē×ÓÓÉøŗ¼«¾µ¼ĻßĮ÷ĻņÕż¼«£»
£Ø2£©øŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬ZnŹ§Č„µē×ÓÉś³ÉŠæĄė×Ó£»
£Ø3£©¼ĘĖćCuµÄĪļÖŹµÄĮ棬½įŗĻµē¼«·“Ó¦Ź½Cu2++2e-=Cu¼ĘĖć×ŖŅʵē×Ó£»
£Ø4£©Ōµē³ŲÖŠµē½āÖŹČÜŅŗŅõĄė×ÓĻņøŗ¼«ŅĘ¶Æ£¬ŃōĄė×ÓĻņÕżĻņŅĘ¶Æ£»
£Ø5£©µē½ā·¢Éś2H2O+4AgNO3$\frac{\underline{\;µē½ā\;}}{\;}$4Ag+O2”ü+4HNO3 £¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČė23.2gŃõ»ÆŅų£¬ĘäĪļÖŹµÄĮæĪŖ0.1mol£¬ČÜŅŗĒ”ŗĆ»Öø“µ½µē½āĒ°µÄדĢ¬£¬Ōņµē½āÖŠÉś³É0.2molAg£¬øł¾ŻAgŌŖĖŲ»ÆŗĻ¼Ū±ä»Æ¼ĘĖć×ŖŅʵē×Ó£®
½ā“š ½ā£ŗ£Ø1£©ŠæĶŌµē³ŲÖŠ£¬Šæ±ČĶ»īĘĆ£¬ZnÓėĮņĖįĶ·“Ӧɜ³ÉCuÓėĮņĖįŠæ£¬¹ŹŠæĪŖøŗ¼«£¬ĶĪŖÕż¼«£¬Ōµē³ŲÖŠ£¬µē×ÓÓÉøŗ¼«Į÷ĻņÕż¼«£¬¹Źµē×ÓµÄĮ÷ĻņĪŖa”śb£¬¹Ź“š°øĪŖ£ŗa”śb£»
£Ø2£©ZnĪŖøŗ¼«£¬Šæµē¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ Zn-2e-=Zn2+£¬¹Ź“š°øĪŖ£ŗZn-2e-=Zn2+£»
£Ø3£©0.64gĶĪļÖŹµÄĮæĪŖ$\frac{0.64g}{64g/mol}$=0.01mol£¬Óɵē¼«·“Ó¦Ź½Cu2++2e-=CuæÉÖŖ£¬µ¼ĻßÖŠ×ŖŅʵē×ÓĪŖ0.01mol”Į2=0.02mol£¬¹Ź×ŖŅʵē×ÓŹżÄæĪŖ0.02NA£¬¹Ź“š°øĪŖ£ŗ0.02NA £»
£Ø4£©×ó²ąÉÕ±ÖŠŠæŹ§µē×Ó±ä³ÉŠæĄė×Ó£¬Ź¹µĆŠæµē¼«ø½½ü“ųÕżµēŗÉ£¬ĪüŅżŅõĄė×ÓĻņ×ó²ąÉÕ±ŅĘ¶Æ£¬ÓŅ²ąÉÕ±ÖŠĶĄė×ӵƵ½µē×Ó±ä³ÉĶ£¬Ź¹µĆĶµē¼«ø½½ü“ųøŗµēŗÉ£¬ĪüŅżŃōĄė×ÓĻņÓŅ²ąÉÕ±ŅĘ¶Æ£¬¹ŹŃĪĒÅÖŠµÄK+ĻņÓŅ²ąÉÕ±ŅĘ¶Æ”¢Cl-Ļņ×ó²ąÉÕ±ŅĘ¶Æ£¬¹Ź“š°øĪŖ£ŗB£»
£Ø5£©µē½ā·¢Éś2H2O+4AgNO3$\frac{\underline{\;µē½ā\;}}{\;}$4Ag+O2”ü+4HNO3 £¬ĻņĖłµĆČÜŅŗÖŠ¼ÓČė23.2gŃõ»ÆŅų£¬ĘäĪļÖŹµÄĮæĪŖ$\frac{23.2g}{232g/mol}$=0.1mol³ä·Ö·“Ó¦ŗó£¬ČÜŅŗĒ”ŗĆ»Öø“µ½µē½āĒ°µÄדĢ¬£¬ÓÉAgŌ×ÓŹŲŗćæÉÖŖ£¬Ōņµē½āÖŠÉś³É0.2molAg£¬Ōņ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæŹĒ0.2mol”Į£Ø1-0£©=0.2mol£¬¹Ź“š°øĪŖ£ŗ0.2£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éŌµē³ŲµÄ¹¤×÷ŌĄķ”¢µē½āŌĄķ£¬¹Ų¼üĄķ½āÕĘĪÕŌµē³ŲÓėµē½ā¹¤×÷ŌĄķ£¬×¢Ņāµē×Ó×ŖŅĘŹŲŗćŌŁµē»Æѧ¼ĘĖćÖŠÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2H2+O2ØT2H2O | B£® | H++OH-ØTH2O | ||
| C£® | .CaCO3ØTCaO+CO2”ü | D£® | Na2CO3+2HClØT2NaCl+H2O+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaClČÜŅŗ | B£® | ŃĪĖį | C£® | ĮņĖį | D£® | KSCNČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaŗĶO2 | B£® | FeŗĶFeCl3 | C£® | Na2CO3ŗĶHCl | D£® | AlCl3ŗĶNaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 H”¢C”¢N”¢O”¢Al”¢SŹĒ³£¼ūµÄĮłÖÖŌŖĖŲ£®
H”¢C”¢N”¢O”¢Al”¢SŹĒ³£¼ūµÄĮłÖÖŌŖĖŲ£®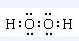 »ņH£ŗC??C£ŗH£®
»ņH£ŗC??C£ŗH£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Ģ«ŃōÄܵē³ŲŹĒĶعż¹āµēŠ§Ó¦»ņÕß¹ā»ÆѧŠ§Ó¦Ö±½Ó°Ń¹āÄÜ×Ŗ»Æ³ÉµēÄܵÄ×°ÖĆ£®Ęä²ÄĮĻ³żµ„¾§¹č£¬»¹ÓŠĶī÷ļŲĪųµČ»ÆŗĻĪļ£®
Ģ«ŃōÄܵē³ŲŹĒĶعż¹āµēŠ§Ó¦»ņÕß¹ā»ÆѧŠ§Ó¦Ö±½Ó°Ń¹āÄÜ×Ŗ»Æ³ÉµēÄܵÄ×°ÖĆ£®Ęä²ÄĮĻ³żµ„¾§¹č£¬»¹ÓŠĶī÷ļŲĪųµČ»ÆŗĻĪļ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ęū³µĪ²ĘųŹĒµ¼ÖĀĖįÓźµÄŌŅņÖ®Ņ» | B£® | ĖįÓź»įŹ¹ĶĮČĄ”¢ŗž²“Ėį»Æ | ||
| C£® | ĖįÓźŠĪ³ÉÖŠ²»Éę¼°Ńõ»Æ»¹Ō·“Ó¦ | D£® | Č¼ĆŗÖŠ¼ÓČėŹÆ»ŅŹÆæÉ·ĄÖĪĖįÓź |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com