
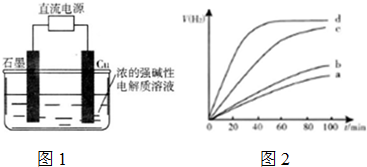
| ʱ��/min | 20 | 40 | 60 | 80 |
| N��O2��/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
���� I����1�����ʱCu������ʧ��������Cu2O��
��2�����������£�N2H4������Cu��OH��2��Ӧ����Cu2O��N2��ˮ������Cu2O��ˮ���ܷ��������ЧӦ��
��3���躬ͭ�����ʵ���Ϊxmol��������ͭ�����ʵ���Ϊymol������������ϵ�͵����غ���ʽ�����ͭ�����ʵ������ټ����ͭ������������
��4�����ݻ�ѧ��Ӧ����֮�ȵ��ڼ�����֮�ȼ��㷴Ӧ���ʣ���ƽ��ʱ����������0.002mol�������Ȼ�ѧ����ʽ���㣻
��5������ͼ�����ߵı仯�����жϣ�����б��Խ��Ӧ����Խ���¶����ߣ�б����С���Դ˽��
��� �⣺I����1�����ʱCu������ʧ��������Cu2O���缫����ʽΪ2Cu+2OH--2e-=Cu2O+H2O���ʴ�Ϊ��2Cu+2OH--2e-=Cu2O+H2O��
��2�����������£�N2H4������Cu��OH��2��Ӧ����Cu2O��N2��ˮ���䷴Ӧ�Ļ�ѧ����ʽΪ��N2H4+4Cu��OH��2=2Cu2O+N2��+6H2O������Cu2O��ˮ��Һ���γɽ��壬���Ը�����Һ�Ƿ���ж����ЧӦ�������Ƿ���������Cu2O��
�ʴ�Ϊ��N2H4+4Cu��OH��2=2Cu2O+N2��+6H2O�������ЧӦ��
��3����״���µ�NO����148mL����NO�����ʵ���Ϊ��$\frac{0.448L}{22.4L/mol}$=0.02mol
�躬ͭ�����ʵ���Ϊxmol��������ͭ�����ʵ���Ϊymol��
64x+144y=3.52g��
2x+2y=0.02��3��
���x=0.01mol��y=0.02mol��
w��Cu2O��=$\frac{0.02mol��144g/mol}{3.52g}$��100%=81.8%��
�ʴ�Ϊ��81.8%��
��4���ɱ������ݿ�֪ǰ20minʱv��O2��=$\frac{\frac{0.0010mol}{2L}}{20min}$=2.5��10-5 mol��L-1��min -1��
��v��H2O��=2v��O2��=5.0��10-5 mol��L-1��min -1����ƽ��ʱ����������0.002mol��������Ҫ���յĹ���Ϊ0.002mol��484kJ•mol-1=0.968kJ��
�ʴ�Ϊ��5.0��10-5 mol��L-1��min -1��0.968��
��5��A��c��d����б�ʽϴ�˵����Ӧ���ʽϴ���c��d�����Ƶõ�Cu2O��Ч����Խϸߣ���A��ȷ��
B������ֻ�ı䷴Ӧ���ʣ���Ӱ��ƽ���ƶ�����B����
C���ò�ͬ�ķ����Ʊ���������ͭ�Ŀ�����С��ͬ����ͼ���֪��Ч����ͬ�����Ч����Cu2O�����Ĵ�ϸ��������Ե��йأ���C��ȷ��
D���¶����ߣ�б����С��˵��Cu2O��ˮ�ֽ�ʱ����Ҫ���˵��¶ȣ���D��ȷ��
�ʴ�Ϊ��ACD��
���� ���⿼���Ϊ�ۺϣ��漰������ͭ���Ʊ�����Ӧ���ʵļ��㡢��ѧƽ���ƶ������ԭ����Ӧ�õȣ�������ѧ���ķ����������Ի���֪ʶ��Ӧ�������ͼ��������Ŀ��飬ע����յ缫����ʽ����д���Ѷ��еȣ�


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�����и�����ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
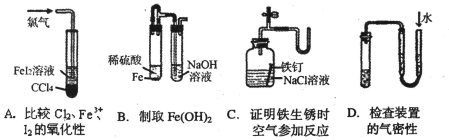
����װ�û�������ܴﵽ ʵ��Ŀ�ĵ���
ʵ��Ŀ�ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ�����и߶���ѧ���ڳ����Ի�ѧ�Ծ� ���ͣ�ʵ����
ijǿ������Һ�п��ܺ��е�������K����NH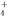 ��Al3����AlO
��Al3����AlO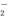 ��SO
��SO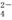 ��SiO
��SiO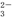 ��CO
��CO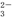 ��Cl���е�ij�������ӣ��ֽ�������ʵ�飺
��Cl���е�ij�������ӣ��ֽ�������ʵ�飺
��ȡ��������Һ�������ữ��Ba��NO3��2��Һ���������ɣ�
����ȡ������Һ�������ᣬ�������ǣ�һ��ʱ�䱣��ԭ����ʼ���������������࣬������������������һ�����壬��������������ʧ��
��1��ԭ��Һ�п϶����� �������ǣ��϶������ڵ������ǡ�
�������ǣ��϶������ڵ������ǡ�
��2����֪һ������ԭ��Һ�м���5mL0��2mol/L����ʱ����������ȫ��ʧ��������������������Һ�ɵõ�����0��187g����ԭ��Һ���Ƿ���Cl�� ����
��3�����շ�Ӧ˳������д�����з�����Ӧ�����ӷ�Ӧ����ʽ
��H����OH����H2O��
��
��HCO3����H����H2O��CO2��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ�����и߶���ѧ���ڳ����Ի�ѧ�Ծ� ���ͣ�ѡ����
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A����KIO3����������Һ�е�KI:5I����IO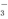 ��3H2O��3I2��6OH��
��3H2O��3I2��6OH��
B����NH4HCO3��Һ�мӹ�����NaOH��Һ�����ȣ�NH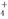 ��OH��?NH3����H2O
��OH��?NH3����H2O
C��������SO2ͨ���䰱ˮ�У�SO2��NH3��H2O��HSO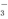 ��NH
��NH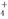
D����ϡ����ϴ���Թ��ڱڵ�������Ag��2H����NO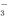 ��Ag����NO����H2O
��Ag����NO����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꼪��ʡ�����и߶���ѧ���ڳ����Ի�ѧ�Ծ� ���ͣ�ѡ����
Ϊ�˳�ȥMgCl2������Һ�е�Fe3�������ڼ��Ƚ���������¼���һ���Լ������˺��ټ������������ᣬ�����Լ���
A�� NH3��H2O
NH3��H2O
B��NaOH
C��Na2CO3
D��MgCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
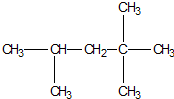 ��Ϊ��������ȼ�ϵ����ͣ�����Ҫ�ɷ��������飬��ṹ��ʽ��ͼ���и�ʽ���Կ϶������������黥��Ϊͬϵ����ǣ�������
��Ϊ��������ȼ�ϵ����ͣ�����Ҫ�ɷ��������飬��ṹ��ʽ��ͼ���и�ʽ���Կ϶������������黥��Ϊͬϵ����ǣ�������| A�� | C2H4 | B�� | C8H18 | C�� | C7H16 | D�� | C6H12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | MgCl2 | Mg��OH��2 | MgCO3 |
| �ܽ�ȣ�g/100g�� | 74 | 0.00084 | 0.01 |
| A�� | ��֪MgCO3��K=6.82��10-6moL-2•L-2�������й���MgCO3����Һ�У�����c��Mg2+��=c��CO32-������c��Mg2+��•c��CO32-��=6.82��10-6moL2-•L-2 | |
| B�� | ����������������ˮ��ϣ����ȡ����գ����յĹ��������ͬ | |
| C�� | ��ȥ�����к��е�MgCl2���ʣ���ѳ����Լ�ΪNa2CO3 | |
| D�� | ��ʯ��ˮ��������Mg2+��HCO3��Ӳˮ�����������ӷ�Ӧ�ķ���ʽΪMg2++2HCO3+Ca2+2OH�TCaCO3��+MgCO3��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
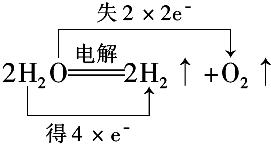 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ������ | B�� | ���ʵ��� | C�� | �������� | D�� | ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com