
【题目】为了探究浓硫酸与蔗糖的炭化产物,设计下图装置进行实验(a和b分別为两个气球)。

已知:CO气体通入氯化钯溶液,溶液变为黑色。
实验过程如下:
I .按图示连接好仪器,然后检验装置的气密性。
II.在双通玻璃管中①②③④处分别放罝滴有酸性高锰酸钾溶液的滤纸、滴有品红溶液的滤纸、浸有氯化钯溶液的滤纸和浸有溴水的滤纸。
III.夹好止水夹K,向三颈烧瓶A中的蔗糖上滴3~4滴蒸馏水,再加入3 mL浓硫酸,玻璃管中③处滤纸由白色变为黑色。
IV.打开止水夹K,使烧瓶内气体缓慢通过B和C装置,一段时间之后,发现④处的滤纸颜色没有发生变化,C中的澄清石灰水变浑浊。
(1)装置A中盛装浓硫酸的仪器名称为______;上述实验体现了硫酸的那些性质_____。
(2)实验步骤III中,向蔗糖上滴水的目的是_________________;
(3)若反应生成两种碳的氧化物相同条件下的体积相同,写出蔗糖炭化后发生反应的化学反应方程式_________。
(4)步骤IV的实验目的是_______________________。
(5)该实验体现了“微型实验”绿色环保的优点,有人建议将装置B改为滴有酸性高锰酸钾溶液的滤纸置于后面的双通玻璃管中,你对该改进建议的评价是_________。
【答案】 分液漏斗 吸水、脱水性、强氧化性 少量水稀释浓H2SO4时放出的热,能加快蔗糖的脱水速度 2C+3H2SO4 (浓) ![]() CO↑+CO2↑+3SO2↑+3H2O 检验产物CO2的存在 酸性离锰酸钾溶液的用量过少,不能保证SO2的完全吸收,影响CO2的检验
CO↑+CO2↑+3SO2↑+3H2O 检验产物CO2的存在 酸性离锰酸钾溶液的用量过少,不能保证SO2的完全吸收,影响CO2的检验
【解析】 (1)装置A中盛装浓硫酸的仪器为分液漏斗;蔗糖上滴3~4滴蒸馏水,再加入3 mL浓硫酸,浓硫酸吸水稀释放热,使蔗糖脱水碳化,浸有氯化钯溶液的滤纸变成黑色,说明生成了一氧化碳,是因为浓硫酸具有强氧化性,该实验体现了硫酸的吸水性、脱水性和强氧化性,故答案为:吸水性、脱水性和强氧化性;
(2)步骤III中,向蔗糖上滴水,稀释浓H2SO4时放出的热,能加快蔗糖的脱水速度,故答案为:少量水稀释浓H2SO4时放出的热,能加快蔗糖的脱水速度;
(3)根据题意,C中的澄清石灰水变浑浊,说明生成了二氧化碳,若反应生成一氧化碳和二氧化碳在相同条件下的体积相同,则蔗糖炭化后发生反应的化学反应方程式为2C+3H2SO4 (浓) ![]() CO↑+CO2↑+3SO2↑+3H2O,故答案为:2C+3H2SO4 (浓)
CO↑+CO2↑+3SO2↑+3H2O,故答案为:2C+3H2SO4 (浓) ![]() CO↑+CO2↑+3SO2↑+3H2O;
CO↑+CO2↑+3SO2↑+3H2O;
(4)步骤IV中生成的气体通过酸性高锰酸钾溶液,除去反应生成的二氧化硫,便于具有是否生成二氧化碳,故答案为:检验产物CO2的存在;
(5) 若酸性离锰酸钾溶液的用量过少,不能保证SO2的完全吸收,影响CO2的检验,故答案为:酸性离锰酸钾溶液的用量过少,不能保证SO2的完全吸收,影响CO2的检验。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是:
A. l6O与 l8O的转化可以通过化学反应实现
B. 灼烧氯化钠时火焰呈黄色,那是发生了化学反应
C. 碱性氧化物一定是金属氧化物
D. 只由一种元素组成的物质一定是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 铜跟硝酸银溶液反应:Cu+Ag+===Cu2++Ag
B. 碳酸钙与盐酸反应:![]() +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
C. 硫酸与氢氧化钡溶液反应:H++![]() +Ba2++OH===BaSO4↓+H2O
+Ba2++OH===BaSO4↓+H2O
D. Ba(OH)2与CuSO4溶液反应:Cu2++![]() +Ba2++2OH===BaSO4↓+Cu(OH)2↓
+Ba2++2OH===BaSO4↓+Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 煤的干馏、煤的气化和液化都是化学变化,石油的分馏是物理变化
B. 葡萄糖与果糖、淀粉与纤维素分子式相同结构不同,均互为同分异构体
C. 只有一种元素组成的物质一定是纯净物
D. 单质硅可用于制造硅太阳能电池以及光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是
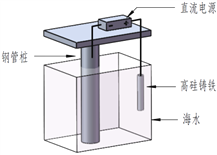
A. 通入保护电流使钢管桩表面腐蚀电流接近于零
B. 通电后外电路电子被强制从高硅铸铁流向钢管桩
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com