
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 将钠投入到硫酸铜溶液中发生的反应:2Na+Cu2+=2Na++Cu | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
分析 A.漏掉了钡离子与硫酸根离子的反应;
B.钠与硫酸铜溶液反应不会置换出铜;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.碳酸钙与稀盐酸反应生成氯化钙、二氧化碳气体和水.
解答 解:A.氢氧化钡与硫酸反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A错误;
B.钠投入硫酸铜溶液中,钠先与水反应生成氢氧化钠和氢气,然后铜离子与氢氧化钠溶液反应,正确的离子反应为:2Na+2H2O+Cu2+═Cu(OH)2↓+2Na++H2↑,故B错误;
C.铜片插入硝酸银溶液中发生置换反应,正确的离子方程式为:Cu+2Ag+═Cu2++2Ag,故C错误;
D.碳酸钙溶于稀盐酸中,反应的离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 已知2SO2(g)+O2(g)?2SO3(g)△H=-196.64kJ•mol-1,在容器中充入1mol SO2和0.5mol O2充分反应,放出的热量为98.32KJ | |
| C. | 已知在120C、101kPa时,1gH2燃烧生成水蒸气放出121KJ,其热化学方程式表示为H2(g)+$\frac{1}{2}$O2(g)=2H2O(l)△H=-242KJ/mol | |
| D. | CO(g) 的燃烧热是283.0kJ•mol-1,则CO2(g)=CO(g)+$\frac{1}{2}$O2(g)△H=+283kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:6:0 | B. | 4:3:1 | C. | 3:3:2 | D. | 7:6:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀硫酸与氧化铜反应:O2-+2H+═H2O | |
| B. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 碳酸钡与盐酸反应:BaCO3+2H+═Ba2++CO2↑+H2O | |
| D. | 向氯化钙溶液中通入CO2:Ca2++H2O+CO2═CaCO3↓+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
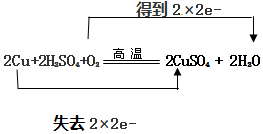 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成该电池的正极和负极必须是两种活性不同的金属 | |
| B. | 放电时每消耗1 mol CH3OH转移12 mol电子 | |
| C. | 放电时电解质溶液的pH逐渐增大 | |
| D. | 放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 焓减少的反应一定可以自发进行 | B. | 焓增加的反应可能自发进行 | ||
| C. | 熵增加的反应一定可以自发进行 | D. | 熵减少的反应一定不能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈黄绿色,说明氯水中含有Cl2 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 向NaBr溶液中滴加氯水,溶液颜色变成黄色,说明氯水中含有HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气的摩尔质量是17g | |
| B. | NA个氢分子和NA个氧分子的质量比为1:16 | |
| C. | 标准状况下,22.4 L水中含有的分子数目为NA | |
| D. | 100 mL1mol/L MgCl2溶液中含有 0.1 mol Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com