
在密闭容器里,A与B反应生成C,其反应速率分别用VA、VB、VC表示,已知2VB=3VA、3 VC =2 VB,则此反应可表示为( )
A. 2A+3B=2C B. A+3B=2C C. 3A+B=2C D. A+B=C
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
某探究小组研究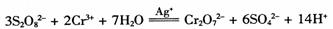 的反应速率与浓度的关系。反应速率v(Cr3+)可通过测定c(Cr3+)减半所需时间来确定。在一定温度下,获得如下实验数据:
的反应速率与浓度的关系。反应速率v(Cr3+)可通过测定c(Cr3+)减半所需时间来确定。在一定温度下,获得如下实验数据:
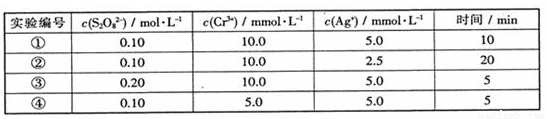
分析以上数据所得出的结论不正确的是
A、增大c(Ag+),v(Cr3+)增大
B、实验②的v(Cr3+)为0.25mmol•L-1•min-1
C、增大c(S2O82-),v(Cr3+)增大
D、增大c(Ag+),v(Cr3+)不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上教学质检化学试卷(解析版) 题型:选择题
下列分子中,属于含有极性键的非极性分子的一组是
A.SO2、CCl4 B.BF3、CO2 C.H2、N2 D.NH3、H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:选择题
吸热反应C+CO2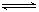 2CO反应速率为 ?1,放热反应N2+3H2
2CO反应速率为 ?1,放热反应N2+3H2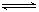 2NH3反应速率为 ?2,对于上述反应,当温度升高时,?1和
2NH3反应速率为 ?2,对于上述反应,当温度升高时,?1和 ?2的变化情况为? ?
?2的变化情况为? ?
A.同时增大  B.同时减小
B.同时减小
C.增大,减小 D.减小,增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:选择题
下列各变化中不属于原电池的反应的是( )
A.为防止轮船外壳生锈,在船底装上锌块
B.镀锌铁表面锌有划损时,也能阻止铁被氧化
C.在空气中金属铝表面迅速氧化形成保护层
D.锌和稀硫酸反应时,加入少量的CuSO4溶液可使反应加快
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| A. | 5.7×10-18 mol•L-1 | B. | 2.6×10-5mol•L-1 | ||
| C. | 1.6×10-13mol•L-1 | D. | 5.7×10-24mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸中的HNO3见光会分解,因此有时在实验室看到的浓硝酸呈黄色 | |
| B. | SO2具有漂白性,因此可使溴水褪色 | |
| C. | Na的金属性比Cu强,因此可用Na与CuSO4溶液反应制取Cu | |
| D. | Fe在Cl2中燃烧生成FeCl3,因此在与其他非金属反应的产物中Fe也显+3价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com