
【题目】(1)2017年中科院某研究团队通过设计一种新型Na-Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1 = -aKJ/mol
C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2= -bKJ/mol
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式_________________________________。
(2)利用CO2及H2为原料,在合适的催化剂(如Cu/ZnO催化剂)作用下,也可合成CH3OH,涉及的反应有:
甲:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
CH3OH(g)+H2O(g) △H= — 53.7kJ·mol-1 平衡常数K1
乙:CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
CO(g)+H2O(g) △H= + 41.2kJ·mol-1 平衡常数K2
①CO(g)+2H2(g) ![]() CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应△H_____0(填“大于”或“小于”)。
CH3OH(g)的平衡常数K=______(用含K1、K2的表达式表示),该反应△H_____0(填“大于”或“小于”)。
②提高CO2转化为CH3OH平衡转化率的措施有___________(填写两项)。
③催化剂和反应体系的关系就像锁和钥匙的关系一样,具有高度的选择性。下列四组实验,控制CO2和H2初始投料比均为1:2.2,经过相同反应时间(t1min)。
温度(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) | 综合选项 |
543 | Cu/ZnO纳米棒材料 | 12.3 | 42.3 | A |
543 | Cu/ZnO纳米片材料 | 11.9 | 72.7 | B |
553 | Cu/ZnO纳米棒材料 | 15.3 | 39.1 | C |
553 | Cu/ZnO纳米片材料 | 12.0 | 70.6 | D |
由表格中的数据可知,相同温度下不同的催化剂对CO2的转化为CH3OH的选择性有显著影响,根据上表所给数据结合反应原理,所得最优选项为___________(填字母符号)。
(3)以CO、H2为原料合成甲醇的反应为:CO(g)+2H2(g)![]() CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
CH3OH(g)。在体积均为2L的三个恒容密闭容器Ⅰ、Ⅱ、Ⅲ中,分别都充入1molCO和2molH2,三个容器的反应温度分别为T1、T2、T3且恒定不变。下图为三个容器中的反应均进行到5min时H2的体积分数示意图,其中有一个容器反应一定达到平衡状态。
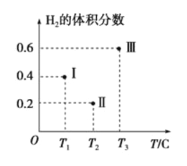
①0~5min时间内容器Ⅱ中用CH3OH表示的化学反应速率为_________________。
②三个容器中一定达到平衡状态的是容器________(填写容器代号)。
【答案】8CO2(g)+25H2(g)=C8H18(1)+16H2O(1) ΔH=—(25a-b)KJ/mol K=![]() 小于 降低温度、减小产物浓度 B 0.0875mol/(L·min) Ⅲ
小于 降低温度、减小产物浓度 B 0.0875mol/(L·min) Ⅲ
【解析】
(1)已知:①H2(g)+1/2O2(g)=H2O(l) ΔH1 =—aKJ/mol;
②C8H18(1)+25/2O2(g)=8CO2(g)+9H2O(1) ΔH2=—bKJ/mol
根据盖斯定律,由①×25-②得反应方程式:8CO2(g)+25H2(g)=C8H18(1) +16H2O(1) ΔH=25ΔH1-ΔH2=ΔH=—(25a-b)KJ/mol;
(2) ①已知甲:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-53.7 kJ·mol-1平衡常数K1
CH3OH(g)+H2O(g)△H=-53.7 kJ·mol-1平衡常数K1
乙:CO2(g)+H2(g)![]() CO(g)+H2O(g)△H=+41.2 kJ·mol-1平衡常数K2;根据盖斯定律,由甲-乙得反应CO(g)+2H2(g)
CO(g)+H2O(g)△H=+41.2 kJ·mol-1平衡常数K2;根据盖斯定律,由甲-乙得反应CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=
CH3OH(g)的平衡常数K=![]() ;△H=-53.7 kJ·mol-1-41.2 kJ·mol-1=-94.9 kJ·mol-1<0;②反应CO(g)+2H2(g)
;△H=-53.7 kJ·mol-1-41.2 kJ·mol-1=-94.9 kJ·mol-1<0;②反应CO(g)+2H2(g) ![]() CH3OH(g)是气体体积缩小的放热反应,提高CO2转化为CH3OH平衡转化率的措施有降低温度、减少产物浓度、按比例充入原料CO2和H2等;③由表中数据分析在相同温度下不同催化剂对甲醇的选择性有显著影响,使用Cu/ZnO纳米片催化剂时甲醇选择性高;使用相同的催化剂在不同温度下,虽然二氧化碳的转化率增加,甲醇的选择性却减小,说明温度升高,副产物增加,因此综合考虑选B选项;
CH3OH(g)是气体体积缩小的放热反应,提高CO2转化为CH3OH平衡转化率的措施有降低温度、减少产物浓度、按比例充入原料CO2和H2等;③由表中数据分析在相同温度下不同催化剂对甲醇的选择性有显著影响,使用Cu/ZnO纳米片催化剂时甲醇选择性高;使用相同的催化剂在不同温度下,虽然二氧化碳的转化率增加,甲醇的选择性却减小,说明温度升高,副产物增加,因此综合考虑选B选项;
(3) ①CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
开始时的物质的量:1 2 0
转化的物质的量: a 2a a
平衡时的物质的量:1-a 2-2a a
容器Ⅱ中0~5 min内H2含量是20%,a=![]() ,v(CH3OH)= 0.0875mol/(L·min);②Ⅲ中温度高氢气含量高,说明达到平衡升高温度平衡逆向移动,氢气含量增加。
,v(CH3OH)= 0.0875mol/(L·min);②Ⅲ中温度高氢气含量高,说明达到平衡升高温度平衡逆向移动,氢气含量增加。


科目:高中化学 来源: 题型:
【题目】某温度时,在一容积为1L的密闭容器中,加入0.4 mol的N2和1.2 mol的H2,在一定条件下发生如下反应:N2(B)+3H2(g)![]() 2NH3(g) △H<0,5min 时达到平衡,反应中NH3的物质的量浓度的变化情况如图所示:
2NH3(g) △H<0,5min 时达到平衡,反应中NH3的物质的量浓度的变化情况如图所示:

请回答下列问题:
(1) 根据如图,计算从反应开始到平衡时,平均反应速率v(N2)=_________。
(2) 该反应的化学平衡常数表达式为__________________。
(3) 反应达到平衡后,第5min末保持其他条件不变,若改变反应温度,则NH3的物质的量浓度不可能为_________(填序号)。
A.0.80mol·L-1 B.0.25mol·L-1 C.0.20mol·L-1 D.0.08mol·L-1
(4) 反应达到平衡后,第5 min末保持其他条件不变,若只把容器的体积缩小一半,平衡移动_________(填“向右”、“向左”或“不”,化学平衡常数_________( 填“增大”、“减少”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的表示方法多种多样,下面是常用的有机物的表示方法:
①![]() ②
② ③CH4 ④
③CH4 ④  ⑤
⑤![]()
⑥

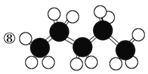

⑩
(1)上述表示方法中属于结构简式的为__________;
属于结构式的为________;
属于键线式的为________;
属于比例模型的为________;
属于球棍模型的为________。
(2)写出⑨的分子式:________。
(3)写出⑩中官能团的电子式:________、________。
(4)②的分子式为________,最简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于很多人来说,喝茶是人生的一大乐事,茶叶中含有少量的咖啡因。咖啡因具有扩张血管、刺激心脑等作用,在100 ℃时失去结晶水并开始升华,120 ℃时升华相当显著,178 ℃时升华很快。其结构简式如图所示。

实验室可通过下列简单方法从茶叶中提取咖啡因:

(1)咖啡因的分子式为___________。
(2)步骤1浸泡茶叶所用的溶剂最好为___________(填序号)。
A.水 B.乙醇 C.石油醚
(3)步骤1、步骤4所进行的操作或方法分别是______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是一种具有果香味的合成香料,下图为合成X的某种流程:

提示:①![]() 不能最终被氧化为—COOH;
不能最终被氧化为—COOH;
②D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)C分子中官能团的名称是__________,E的结构简式是________。
(2)D+E→X的化学反应类型为________反应。
(3)上述A、B、C、D、E、X六种物质中,互为同系物的是____________________。
(4)C的一种同分异构体F可以发生水解反应,则F的结构简式为________、 ________。
(5)反应C+E→X的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为探究草酸亚铁(FeC2O4)的热分解产物,按下面所示装置进行实验。以下说法错误的是

A. 实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO气体
B. 反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3
C. 装置C的作用是除去混合气中的CO2
D. 反应结束后,应熄灭A、E处酒精灯后,持续通入N2直至温度恢复至室温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)指出如下图实验装置中的错误之处。(加热装置中烧杯底部已垫有石棉网)

①_____________________________________;②_______________________________________。
(2)右图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。

a.玻璃棒用作引流 b.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
c.将滤纸湿润,使其紧贴漏斗壁 d.滤纸边缘高出漏斗
Ⅱ.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请回答下列问题:

(1)指出提取碘的过程中有关实验操作①和③的名称:__________;________。
(2)在3 mL碘水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是下图中的________(注:试管中深色区为有色溶液),下层_____色。

Ⅲ.某溶液中含有MgSO4和Na2SO4两种溶质,选择适当试剂将溶液中的镁离子转化为沉淀或固体分离出来,设计实验流程如下:

(1)欲证明滤液中存在SO42-、OH -,选用的方案是先取少量的滤液滴加________,发现溶液变红,再向其中加入________溶液,出现白色沉淀,则可证明SO42-、OH - 均存在。
(2)如何洗涤Mg(OH)2沉淀?___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中粒子的物质的量浓度关系正确的是( )
A. 0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO![]() )>c(HCO
)>c(HCO![]() )>c(OH-)
)>c(OH-)
B. 20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH![]() )+c(OH-)
)+c(OH-)
D. 0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中: c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com