
����Ŀ��������һ����Ҫ�Ļ�����Ʒ���������������Ϊһ�����ҹ�ҵ����ˮƽ��һ�ֱ�־����Ӧ2SO2��O2![]() 2SO3�ǹ�ҵ��ȡ�������Ҫ��Ӧ֮һ������˵������ȷ����(����)
2SO3�ǹ�ҵ��ȡ�������Ҫ��Ӧ֮һ������˵������ȷ����(����)
A. �÷�ӦΪ���淴Ӧ����һ�������¶������������������ȫ��ת��Ϊ��������
B. �ﵽƽ���Ӧ��ֹͣ�ˣ������淴Ӧ��������Ҷ�Ϊ��
C. ������������Ӧ������������ʱ��Ҫ�����ʵ�����ѧ��Ӧ����
D. ������������Ӧ������������ʱ��Ҫ����ʹ�����ܶ�Ķ�������ת��Ϊ��������
���𰸡�B
��������A�����淴Ӧ����һ�������²��ܽ��г��ķ�Ӧ������Ӧ���淴Ӧͬʱ���У��÷�ӦΪ���淴Ӧ������һ��������SO2��O2������ȫ��ת��ΪSO3 ��ѡ��A��ȷ��B���ﵽƽ�������Ӧ���ʺ��㷴Ӧ������ͬ���Ƕ�̬ƽ�⣬���ʲ���Ϊ0��ѡ��B����ȷ��C��������������Ӧ������������ʱ��Ҫ�����ʵ�����ѧ��Ӧ���ʣ����������Ч�ʣ�ѡ��C��ȷ��D��������������Ӧ������������ʱ��Ҫ����ʹ�����ܶ�Ķ�������ת��Ϊ����������߶�������������ʣ���С��Ⱦ��ѡ��D��ȷ����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g��+H2��g��CO��g��+H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ��
��2���÷�ӦΪ��Ӧ��ѡ����ȡ��������ȡ�����
��3��830��ʱ�������еķ�Ӧ�Ѵﵽƽ�⣮�������������������£����������������ƽ���ƶ���ѡ�������Ӧ���������淴Ӧ��������������
��4���� 830��ʱ���������г���1mol CO��5mol H2O����Ӧ�ﵽƽ����仯ѧƽ�ⳣ��K1.0��ѡ����ڡ�����С�ڡ��������ڡ���
��5����1200��ʱ����ijʱ��ƽ����ϵ��CO2��H2��CO��H2O��Ũ�ȷֱ�Ϊ2molL��1��2molL��1��4molL��1��4molL��1 �� ���ʱ������Ӧ��ƽ���ƶ�����Ϊ �� ��ѡ�����Ӧ�������淴Ӧ���������ƶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CrO42-+2H+![]() Cr2O72-+H2O��25��ʱ,���ڳ�ʼŨ��Ϊ1.0mol��L-1��Na2CrO4��Һ��pH,�ⶨƽ��ʱ��Һ��c(Cr2O72-)��c(H+),����������ߡ�����˵������ȷ������ ��
Cr2O72-+H2O��25��ʱ,���ڳ�ʼŨ��Ϊ1.0mol��L-1��Na2CrO4��Һ��pH,�ⶨƽ��ʱ��Һ��c(Cr2O72-)��c(H+),����������ߡ�����˵������ȷ������ ��

A. ƽ��ʱ,pHԽС,c(Cr2O72-)Խ��
B. A��B����c(CrO42-)֮��Ϊ5��2
C. B��CrO42-��ƽ��ת����Ϊ40%
D. ƽ��ʱ,����Һ��c(CrO42-)=2c(Cr2O72-),��c(H+)=1.0��10-7mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҳɹ���������Яʽ����������ȼ�ϵ�أ����Ա�������Ϊȼ�ϣ�����Ϊ��������������ǹ�̬�����������״̬���ܴ���O2���� �õ�ص��ܷ�Ӧ��C3H8+5O2�T3CO2+4H2O��������ӦΪC3H8��20e��+10O2���T3CO2+4H2O�����й��ڸ�ȼ�ϵ�ص�˵������ȷ���ǣ�������
A.�����ڵ�����У�O2���ɸ�����������
B.��ص�����ͨ�����
C.��·��ÿͨ��5 mol ���ӣ�Լ��5.6 L��״���µı��鱻��ȫ����
D.�ڵ�������ĵ缫��ӦΪO2��4e���T2O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Һ��ȷ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A. �����ʵ���Ũ�ȵ�CuSO4��(NH4)2SO4�Ļ����Һ![]()
B. 0.2 mol/L NaHCO3��Һ��0.1 mol/LNaOH��Һ��������ϣ�![]()
C. pH=2��������pH=12�İ�ˮ��������![]()
D. 0.1 mol/LCH3COONa��Һ��ͨ��HC1���壬��pH=7(��Һ����仯���Բ���)��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CoCO3��һ������﮵�ص缫��ԭ�ϡ��Ժ��ܷ�������Ҫ�ɷ�CoO��Co2O3��������Al2O3��ZnO�����ʣ�Ϊԭ���Ʊ�CoCO3��һ�ֹ����������£�
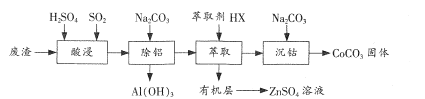
�±��г�����ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0 mol/L���㣩

(1)�������ʱͨ��SO2��Ŀ����__��
(2)��������ʱ������ҺpH��ΧΪ__���ù�������Ҫ��Ӧ�����ӷ���ʽΪ__��
(3)����ȡ�����̿ɱ�ʾΪZnSO4��ˮ�㣩+2HX���л��㣩![]() ZnX2���л��㣩+H2SO4��ˮ�㣩�����л����ȡZnSO4��Һ�IJ�����__��
ZnX2���л��㣩+H2SO4��ˮ�㣩�����л����ȡZnSO4��Һ�IJ�����__��
(4)�����ܡ�ʱNa2CO3��Һ�軺���μӵ�ԭ���� __��
(5)CoCO3�����������տ�������Co2O3���÷�Ӧ�Ļ�ѧ����ʽΪ_______ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������̵�����ã���ϳ�·������ͼ���£�
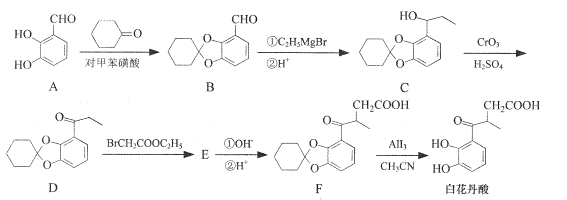
(1)A�еĺ�������������Ϊ__��_____��
(2)C-D�ķ�Ӧ����Ϊ ___��
(3)����������л���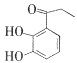 ��д��ͬʱ�������������ĸ��л����һ��ͬ���칹��Ľṹ��ʽ��____��
��д��ͬʱ�������������ĸ��л����һ��ͬ���칹��Ľṹ��ʽ��____��
�ٷ����������ֲ�ͬ��ѧ�������⣻����FeCl3��Һ�ܷ�����ɫ��Ӧ����1 mol�������������3 mol NaOH��Ӧ��
(4)E�Ľṹ��ʽΪ ___��
(5)��֪��![]() ��������֪ʶ����������Ϣд����
��������֪ʶ����������Ϣд����![]() ��CH3CH2OHΪԭ���Ʊ�
��CH3CH2OHΪԭ���Ʊ�![]() �ĺϳ�·������ͼ(�ϳ�·������ͼʾ�����������)____��
�ĺϳ�·������ͼ(�ϳ�·������ͼʾ�����������)____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȹ��ɽ������ʼ���������ҽ���������Ź㷺��Ӧ�á�
(1)��̬ԭ�����ļ۵����Ų�ʽΪ_______��
(2)����ҩ��ɳ�����������Ҷ��Წ���Ľṹ��ʽ��ͼ��ʾ��

�ٷ����е�ԭ�ӹ�����ӻ�������_________��C��N��O����Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ_____��
��1 mol�Ҷ�������к��ЦҼ�����ĿΪ________________��
(3)̼����[La2(CO3)3]���������Ƹ���Ѫ֢��д����CO32-��Ϊ�ȵ������һ�ַ��ӵĻ�ѧʽ�� _______��
(4)�����Ͻ�����ڴ��⣬����֮�����þ���Ļ�ѧʽΪLaNi5(H2)3���侧�����С�ظ��ṹ��Ԫ��ͼ��ʾ����O�����������֮�����е�����������ͼ�С����������_______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ű���ɴ��������ˮ�д�ϴ����������ɰ���ϵ�ճ�����ʺ�ϴ���İ��õ��Լ��ֱ���
A. ��Һ���յ���ȾҺ B. ˫�����Լ�����Һ
C. �Ǽ�����Һ���յ���ȾҺ D. ��Һ������Լ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com