
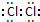 ;
;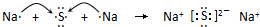 .
. 分析 一般来说,活泼金属与非金属形成离子键,非金属性之间形成共价键,含离子键的一定为离子化合物,以此来解答.
解答 解:(1)其中只含非极性键的物质是氯气,其电子式为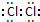 ,故答案为:
,故答案为: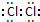 ;
;
(2)其中只由极性键构成的物质是次氯酸,化学式为:HClO,故答案为:HClO;
(3)其中由离子键和共价键构成的物质是过氧化钠中氧氧之间存在非极性键,钠离子与过氧根离子之间是离子键,氯化铵中铵根离子与氯离子之间是离子键,铵根中氮与氢之间是共价键,故答案为:Na2O2、NH4Cl;
(4)H2O2属于共价化合物,氧氧之间存在非极性键,其结构式为H-O-O-H,分子中含有的共价键类型有氧氢极性键和氧氧非极性键,故答案为:H-O-O-H;极性键、非极性键;
(5)Na2S的形成过程为: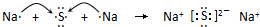 ,故答案为:
,故答案为: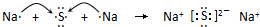 .
.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:实验题
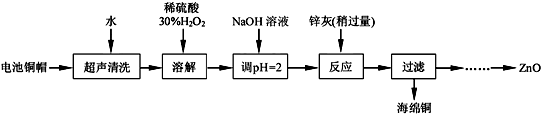
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀的pH | 3.2 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物可能含共价键 | B. | 共价化合物可能含离子键 | ||
| C. | 离子化合物中只含离子键 | D. | 共价化合物中只含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 B原子的核外电子排布式1s22s22p63s23p2,C原子的价电子排布式3s23p5.C原子结构示意图
B原子的核外电子排布式1s22s22p63s23p2,C原子的价电子排布式3s23p5.C原子结构示意图
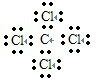 ,结构式
,结构式 ,中心原子Asp3杂化,立体构型是非极性 (填“极性”或“非极性”)分子.
,中心原子Asp3杂化,立体构型是非极性 (填“极性”或“非极性”)分子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.2mol•(L•min) -1 | B. | 18mol•(L•min)-1 | C. | 0.6mol•(L•min) -1 | D. | 0.4mol•(L•min)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 被鉴别的物质 | 鉴别物质(或鉴别方法) | 现象(填入序号即可) |
| 新制氢氧化铜 | ||
| 碘水 | ||
| 硝酸 | ||
| 灼烧 | ||
| 银氨溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚烷(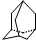 )分子中含有4个 )分子中含有4个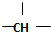 | |
| B. | 利用核磁共振氢谱可以鉴别乙醇和二甲醚 | |
| C. | 高聚物的相对分子质量不一定为单体相对分子质量的整数倍 | |
| D. | 苯、甲苯、乙苯、三硝基甲苯等都是芳香烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com