
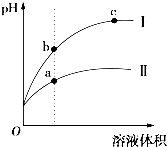
 某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示.据图判断不正确的是( )
某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示.据图判断不正确的是( )| A、I是盐酸,Ⅱ是醋酸 |
| B、溶液的导电性a>b>c |
| C、a、b、c三点KW的数值相同 |
| D、稀释前等体积的 I、Ⅱ溶液中和氢氧化钠的能力相同 |


科目:高中化学 来源: 题型:
| A、溴化钠只有一部分反应,氟化钠未反应 |
| B、氟化银溶于水 |
| C、沉淀是氟化银 |
| D、沉淀是氟化银与溴化银的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 氢氧化钠溶液 | 分液 |
| B | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
| D | 乙炔(硫化氢) | 硫酸铜 | 洗气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
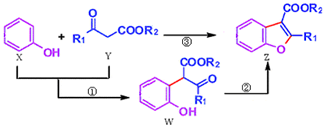
| A、反应①属于加成反应 |
| B、W中至少含有3种官能团 |
| C、X、Y、W、Z中至少有一种物质不能与NaOH溶液反应 |
| D、可用溴水鉴别X和W |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中C、H、O个数之比为1:4:4 |
| B、分子中C、H个数之比为1:2 |
| C、分子中可能含有氧原子 |
| D、此有机物的最简式为CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6 |
| B、C4H8O2 |
| C、C3H10O |
| D、C5H10O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
| Cl2 |
| 460℃ |
| 蒸馏 |
| H2 |
| 1100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
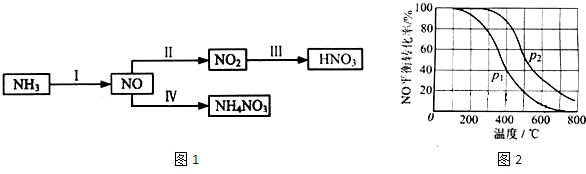
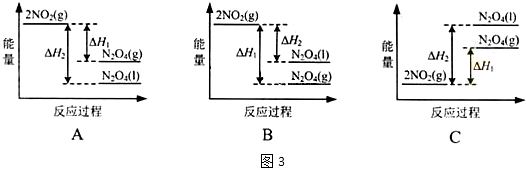
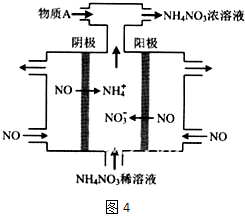
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com