
 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:
一定条件下,可逆反应C(s) + CO2(g)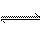 2CO(g) △H>0,达到平衡状态,现进行如下操作:①升高反应体系的温度; ②增加反应物C的用量; ③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是
2CO(g) △H>0,达到平衡状态,现进行如下操作:①升高反应体系的温度; ②增加反应物C的用量; ③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是
A、①②③④ B、①③ C、①②③ D、①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L密闭容器中,充入1 mol N2和3mol H2,一定条件下发生合成氨反应,2min时达到平衡。测得平衡时N2的转化率为40%,求:
(1)NH3的平衡浓度
(2)求该温度下的平衡常数K(分别用N2、H2、NH3的浓度表示,不用计算出结果)
(3)H2在平衡混合气体中的体积分数
(4)平衡时容器的压强与起始时压强之比
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示反应N2(g)+3H2(g)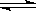 2NH3(g);ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图如下,则氨的百分含量最高的一段时间是
2NH3(g);ΔH=-92.2kJ/mol。在某段时间t0~t6中反应速率与反应过程的曲线图如下,则氨的百分含量最高的一段时间是
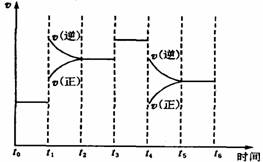
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A.1∶9 B.1∶1 C.1∶2 D.1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,现有一瓶稀氨水、标准盐酸、pH试纸、必要的酸碱指示剂等药品,要测定NH3·H2O电离度(= )的数值,其实验方案可设计如下:
常温下,现有一瓶稀氨水、标准盐酸、pH试纸、必要的酸碱指示剂等药品,要测定NH3·H2O电离度(= )的数值,其实验方案可设计如下:
⑴先测稀氨水的 ,设其数值为a,可通过 实验(写名称,不用写过程)实现此目的。
⑵再测定其pH,设其数值为b,其操作过程简述如下:
⑶用a、b表示该氨水的电离度 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在固定容积的密闭容器中发生可逆反应H2(g)+I2(g) 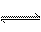 2HI(g)。已知H2和I2的起始浓度均为0.1 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均为0.2 mol/L,则平衡时H2的浓度(mol/L)为
2HI(g)。已知H2和I2的起始浓度均为0.1 mol/L,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均为0.2 mol/L,则平衡时H2的浓度(mol/L)为
A.0.16 B.0.08 C.0.04 D.0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置不能达到实验目的的是 ( )
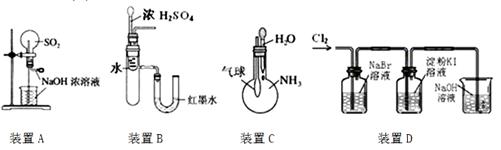
A.用装置A来做SO2的喷泉实验
B.用装置B来验证浓H2SO4与水混合的热量变化
C.用装置C来验证NH3易溶于水
D.用装置D来验证氧化性:Cl2>Br2>I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com