
科目:高中化学 来源:物理教研室 题型:022
现有四组离子,每组有两种金属离子。请各选一种试剂,将它们两者分开。可供选择的试剂有:
A.硫酸 B.盐酸 C.硝酸 D.氢氧化钠溶液 E.氨水
根据上述内容填写下表:
离子组 选用试剂(字母代号) 沉淀物化学式 保留在溶液中的离子
①Zn2+和Al3+
②Zn2+和Mg2+
③Zn2+和Ba2+
④Mg2+和Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:022
已知向含有Zn2+的溶液中滴加氨水,有白色沉淀Zn(OH)2生成,继续滴加氨水使其过量,沉淀溶解,生成了[Zn(NH3)4](OH)2。此外,Zn(OH)2既可溶于盐酸,又可溶于过量的NaOH溶液,生成ZnO22-,所以Zn(OH)2是一种两性氢氧化物。
现有四组离子,每组有两种金属离子。请各选一种试剂,将它们两者分开。可供选择的试剂有:
A.硫酸 B.盐酸 C.硝酸 D.氢氧化钠溶液 E.氨水
根据上述内容填写下表:
离子组 选用试剂(字母代号) 沉淀物化学式 保留在溶液中的离子
①Zn2+和Al3+
②Zn2+和Mg2+
③Zn2+和Ba2+
④Mg2+和Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
晶体硅是一种重要的非金属材料。制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅。
![]() ②粗硅与干燥HCl气体反应制得SiHCl3: Si + 3HCl SiHCl3 + H2
②粗硅与干燥HCl气体反应制得SiHCl3: Si + 3HCl SiHCl3 + H2
③ SiHCl3与过量H2在1000~1100℃反应制得纯硅。
已知SiHCl3能与H2O强烈反应,在空气中易自燃。
请回答下列问题:
(1)第①步制备粗硅的化学反应方程式为 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量
SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为:
。
(3)用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):
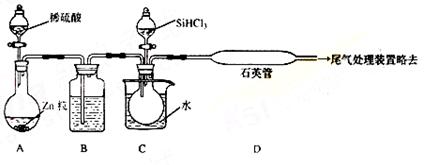
①装置B中的试剂是 ,装置C中的烧瓶需要加热,
其目的是: 。
②装置D不能采用普通玻璃管的原因是 ,
装置D中发生反应的化学方程式为 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)常温下,高锰酸钾晶体遇浓盐酸会生成一种气体,该气体是由瑞典化学家舍勒首先发现的。如图所示,将浓盐酸小心滴入Y形管B端。
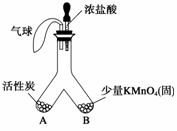
①开始观察到的现象是 。
②一段时间后又可观察到 ,请解释这一现象 。
③应用活性炭的此性质可制作 来达到防毒、防臭的目的(举一例即可)。
(2)①写出CO2和Na2O2反应的化学方程式 。
②某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗? 。
简要说明理由: 。
③该同学无法断定反应中是否有氧气生成,拟使用如图所示装置进行实验(图中铁架台等装置已略去)。
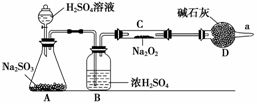
装置中B的作用是 ,
D的作用是 。
④如何证明该同学的两个推断?
。
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是原子序数依次增大的四种短周期元素,已知:W的某种原子没有中子;Y与X相邻,Y与Z也相邻,X、Y、Z三种元素原子的最外层电子数之和为3的整数倍;元素Z在地壳中含量最高。 试回答下列问题:
(1)已知W、Y、Z三种元素两两组合,可组成多种10电子微粒,写出其中两种离子发生反应生成其中两种分子的离子方程式 。
(2)由W、X、Z三种元素可组成A、B、C三种常见的有机化合物,其中A和B是日常生活中常用调味品的主要成分,且A与B能够反应生成C,试写出该反应化学方程式 。
(3)由W、X、Y、Z四种元素的三种元素组成的某种化合物,其浓溶液可与其中第四种元素的单质发生反应,写出该反应的化学方程式 。
(4)由元素X和Z可组成A、B、C、D四种中学化学常见的单质或化合物,四种物质之间存在如右图所示的转化关系。
①写出A与B反应生成C的化学方程式 。

②向50mL 4mol·L-1的NaOH溶液中通入1.12L气体B(标准状况),反应后溶液中溶质的物质的量之比为
。
(5)W、Y、Z三种元素可组成一种无机盐,其组成可表示为W4Y2Z3。该盐溶液中离子浓度由大到小的顺序为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com