
| A. | Z可能是氯化钠 | B. | Z可能是三氧化硫 | C. | X可能是金属铜 | D. | Y不可能是氢气 |
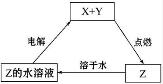
分析 Z的水溶液在电解条件下生成X和Y,X和Y在点燃条件下可生成Z,说明Z在电解条件下,含有的阳离子、阴离子可在电极上放电,且水不参与电极反应,以此解答该题.
解答 解:A.Z可能是氯化钠,X、Y只能为氢气、氯气中的一种,X+Y→Z,2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl,Z电解:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,不符合Z电解生成X、Y条件,故A错误;
B.三氧化硫和水反应SO3+H2O=H2SO4生成硫酸,电解硫酸本质为电解水,电解水生成氢气和氧气,不符合Z电解生成X、Y条件,故B错误;
C.X+Y→Z,Z电解生成X、Y,说明电解电解质本身,所以X可能是金属铜,Y可能为氯气,反应为:X+Y→Z,Cu+Cl2$\frac{\underline{\;点燃\;}}{\;}$CuCl2,Z为CuCl2,电解CuCl2溶液:CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑,故C正确;
D.如Z为HCl,则Y可为氢气,X为氯气,故D错误.
故选C.
点评 本题为高考题,侧重于电解知识的考查,为高频考点,注意注意把握离子的放电顺序以及物质的性质,本题可结合选项提供的物质以及反应的条件进行分析,注意X+Y→Z,Z电解生成X、Y,说明电解电解质本身为解答该题的关键,学习中注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2,NO,HCl,NH3,CO2 | B. | O2,NO,NH3,HCl,SO2 | ||
| C. | NO,O2,NH3,HCl,SO2 | D. | HBr,Cl2,NH3,H2S,C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| B. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果发生了加成反应 | |
| C. | 食品脱氧剂(含铁粉、氯化钠、炭粉等)的脱氧原理与钢铁的吸氧腐蚀相同 | |
| D. | 加入足量氢氧化钠溶液共热,能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 按要求回答下列问题:
按要求回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 pH=2的X、Y、Z三种酸的溶液各1mL,分别稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列正确的是 ( )
pH=2的X、Y、Z三种酸的溶液各1mL,分别稀释到1000mL,其pH与溶液体积(V)的变化关系如图所示,下列正确的是 ( )| A. | X、Y和Z都是弱酸 | B. | 稀释前的浓度大小为c(Z)>c(X)>c(Y) | ||
| C. | 稀释前电离程度大小为X>Y>Z | D. | pH=2时,X、Y、Z都是稀溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com