
| A. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| B. | 使甲基橙变红的溶液中:NH4+、Al3+、NO3-、Cl- | |
| C. | 澄清透明的溶液中:ClO-、MnO4-、Al3+、CH3CH2OH | |
| D. | 0.1mol/L的氯化铁溶液中:Na+、SO42-、Cl-、C6H5OH |
分析 A.在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中存在大量氢离子,硝酸根离子在酸性条件下能够氧化亚铁离子;
B.使甲基橙变红的溶液中存在大量氢离子,四种离子之间不反应,都不与氢离子反应;
C.次氯酸根离子与铝离子之间发生双水解反应,高锰酸根离子能够氧化乙醇;
D.铁离子与苯酚发生络合反应.
解答 解:A.在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液为酸性溶液,Fe2+、NO3-在酸性溶液中发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.使甲基橙变红的溶液为酸性溶液,溶液中存在大量氢离子,NH4+、Al3+、NO3-、Cl-之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.ClO-、Al3+之间发生双水解反应,MnO4-、CH3CH2OH之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.Fe3+、C6H5OH之间发生络合反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于提高学生灵活运用基础知识的能力.


科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
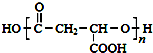 ,合成M的流程图如下:
,合成M的流程图如下: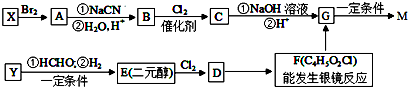
 ,
, .
.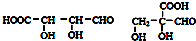 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 B.(CH3)3CCH2CH3 C.
B.(CH3)3CCH2CH3 C. D.正己烷.
D.正己烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向稀盐酸中加入少量钠粒:2Na+2H2O=2Na++2OH-+H2↑ | |
| B. | 将NaHSO4与Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| D. | 往KAl(SO4)2溶液中滴入Ba(OH)2溶液至沉淀的物质的量最大:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在常温下,0.10mol•L-1Na2CO3溶液25mL 用0.10mol•L-1盐酸滴定.当滴定到消耗20mlHCl时所得溶液中离子浓度间的关系有:5c(Cl-)═4c(HCO3-)+4c(CO32-)+4c(H2CO3) | |
| B. | 常温下物质的量浓度相等的①(NH4)2CO3 ②(NH4)2SO4③(NH4)2Fe(SO4)2三种溶液中水的电离程度:③>①>② | |
| C. | 常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:C(CH3COO-)>C(CH3COOH)>C(H+)>C(OH-) | |
| D. | 等体积等物质的量浓度的NaF溶液与NaCl溶液中离子总数:N(NaF)>N(NaCl) |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
贝诺酯是由阿司匹林、扑热息痛经化学法拼合制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下,
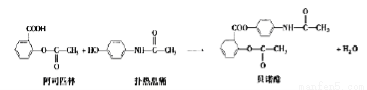
下列叙述错误的是
A.FeCl3溶液可区别阿司匹林和扑热息痛
B.1mol阿司匹林最多可消耗3molNaOH
C.常温下贝诺酯在水中的溶解度大干扑热息痛的
D.扑热息痛发生类似酯水解反应的产物之一分子式为C6H7NO2
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤和石油都是混合物,均由碳和氢两种元素组成 | |
| B. | 液化石油气和天然气的主要成分都是甲烷 | |
| C. | 煤的干馏和石油的分馏发生的都是化学变化 | |
| D. | 用溴的四氯化碳溶液可鉴别分馏获得的汽油和裂化获得的汽油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com