
| 浓度/mol.L-1 时间/min |
c(CO) | c(H2) | c(CH3OH) |
| 0 | 1.0 | 2.0 | 0 |
| 2 | 0.8 | 0.2 | |
| 4 | 1.0 | 0.5 | |
| 6 | 1.0 | 0.5 |
| c(标准液)×V(标准液) |
| V(待测液) |
| 250 |
| 25 |
| 0.225g |
| 0.40g |
| c(标准液)×V(标准液) |
| V(待测液) |


科目:高中化学 来源: 题型:
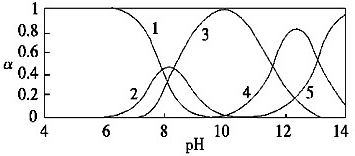
| A、滴加甲基橙溶液呈黄色 | ||||
| B、c(HCO3-)>c(H2CO3)>c(CO32-) | ||||
| C、c(OH-)=c(H+)+c(H2CO3)-c(CO32-) | ||||
D、加水稀释,
|
查看答案和解析>>
科目:高中化学 来源: 题型:
- 3 |
2- 4 |
- 3 |
2- 4 |
c(N
| ||
| c(Pb2+) |
c(N
| ||
| c(Pb2+) |
| 离 子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度/(mg?L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度/(mg?L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 I.将0.050molSO2和0.030molO2放入容积为1L的密闭容器A中;将0.100molSO2和0.060molO2放入容积为1L的密闭容器B中,反应:2SO2(g)+O2(g)?2SO3(g);△H=-196.6kJ?mol-1,恒温恒容下达到平衡时,测得容器A中放出3.932kJ的热量,则容器A中SO2的平衡转化率为
I.将0.050molSO2和0.030molO2放入容积为1L的密闭容器A中;将0.100molSO2和0.060molO2放入容积为1L的密闭容器B中,反应:2SO2(g)+O2(g)?2SO3(g);△H=-196.6kJ?mol-1,恒温恒容下达到平衡时,测得容器A中放出3.932kJ的热量,则容器A中SO2的平衡转化率为| 阳离子 | lgKMY | 阳离子 | lgKMY |
| Na+ | 1.66 | Mn2+ | 13.87 |
| Ca2+ | 10.96 | Pb2+ | 18.04 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2+、Cl-、CO32- |
| B、NH4+、Ba2+、OH- |
| C、S2-、H+、SO32- |
| D、Fe3+、Cl-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2O |
| B、N2O5 |
| C、NO2 |
| D、NO |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、乙酸与碳酸钠溶液反应:2H++CO
| ||||
B、油脂在碱性溶液中水解: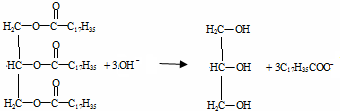 | ||||
C、苯酚钠溶液中通入二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+
| ||||
D、乙醛溶液与足量的银氨溶液共热CH3CHO+2[Ag(NH3)2]++2OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com