
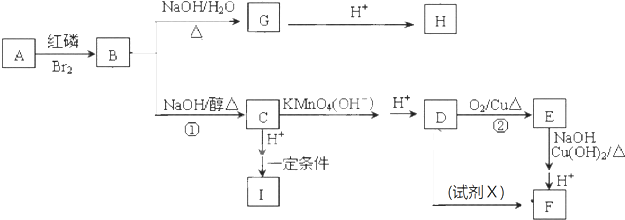
| 红磷 |
| Br2 |

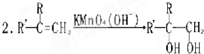
| HBr |
| NaOH |
| 水/△ |
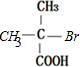 ;B与NaOH的水溶液加热反应生成G,该反应为水解反应,则G为
;B与NaOH的水溶液加热反应生成G,该反应为水解反应,则G为 ;G结构酸化生成H,则H为
;G结构酸化生成H,则H为 ;B在NaOH的醇溶液中加热发生消去反应生成C,则C为
;B在NaOH的醇溶液中加热发生消去反应生成C,则C为 ;C发生信息2反应然后酸化得到D,则D为
;C发生信息2反应然后酸化得到D,则D为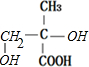 ;D催化氧化生成E:
;D催化氧化生成E: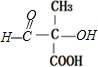 ;E与新制氢氧化铜反应生成F,则F为:
;E与新制氢氧化铜反应生成F,则F为: ,据此进行解答.
,据此进行解答.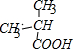 ;A与红磷发生信息1反应生成B,则B为
;A与红磷发生信息1反应生成B,则B为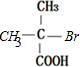 ;B与NaOH的水溶液加热反应生成G,该反应为水解反应,则G为
;B与NaOH的水溶液加热反应生成G,该反应为水解反应,则G为 ;G结构酸化生成H,则H为
;G结构酸化生成H,则H为 ;B在NaOH的醇溶液中加热发生消去反应生成C,则C为
;B在NaOH的醇溶液中加热发生消去反应生成C,则C为 ;C发生信息2反应然后酸化得到D,则D为
;C发生信息2反应然后酸化得到D,则D为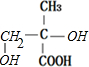 ;D催化氧化生成E:
;D催化氧化生成E: ;E与新制氢氧化铜反应生成F,则F为:
;E与新制氢氧化铜反应生成F,则F为: ,
, 酸化后产物为
酸化后产物为 ,
, 通过加聚反应生成I,则I的链节为:
通过加聚反应生成I,则I的链节为: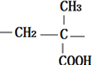 ;
; )分子间脱水可以形成环状化合物分子,化学反应方程式为:2
)分子间脱水可以形成环状化合物分子,化学反应方程式为:2
| 浓硫酸 |
| △ |
 +2H2O,
+2H2O, ;2
;2
| 浓硫酸 |
| △ |
 +2H2O;
+2H2O;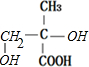 ,D催化氧化生成E:
,D催化氧化生成E: ,所选试剂必须具有强氧化性,可以为:B、重铬酸钾酸性溶液 C、硝酸溶液 E、次氯酸钠 F、高锰酸钾溶液,不能选用的试剂为:A、红磷 D、稀硫酸,
,所选试剂必须具有强氧化性,可以为:B、重铬酸钾酸性溶液 C、硝酸溶液 E、次氯酸钠 F、高锰酸钾溶液,不能选用的试剂为:A、红磷 D、稀硫酸,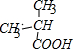 ,A中含有羧基,能够与丙醇反应生酯化反应,生成物分子式为:C7H14O2,其相对分子质量为130;③该有机物能发生银镜反应,分子中含有醛基,苯基与醛基的相对分子质量之和为:77+29=106,其它基态的相对分子质量为:130-106=24,应该为2个C原子,不含有H,说明两个C以碳碳三键连接;②该有机物的核磁共振氢谱有4个峰且峰面积之比为 1:1:2:2,说明该有机物具有对称结构,满足条件的有机物的结构简式为:,
,A中含有羧基,能够与丙醇反应生酯化反应,生成物分子式为:C7H14O2,其相对分子质量为130;③该有机物能发生银镜反应,分子中含有醛基,苯基与醛基的相对分子质量之和为:77+29=106,其它基态的相对分子质量为:130-106=24,应该为2个C原子,不含有H,说明两个C以碳碳三键连接;②该有机物的核磁共振氢谱有4个峰且峰面积之比为 1:1:2:2,说明该有机物具有对称结构,满足条件的有机物的结构简式为:, 、
、 ,
, 、
、 ;
; 水解可以生成HOOCCH2CH2COOH,可以先制备
水解可以生成HOOCCH2CH2COOH,可以先制备 ,
, 可以用
可以用 与NaCN反应制取,
与NaCN反应制取, 可以用乙烯与氯气加成反应获得,乙醇通过消去反应生成乙烯,所以合成路线为:
可以用乙烯与氯气加成反应获得,乙醇通过消去反应生成乙烯,所以合成路线为: ,
, .
.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
| A、该反应的△H>0 |
| B、加压、增大H2浓度和加入催化剂都能提高CO的转化率 |
| C、工业上采用5×103kPa和250℃的条件,其原因是原料气的转化率高 |
| D、t℃时,向1 L密闭容器中投入0.1 mol CO和0.2 mol H2,平衡时CO转化率为50%,则该温度时反应的平衡常数的数值为100 |
查看答案和解析>>
科目:高中化学 来源: 题型:
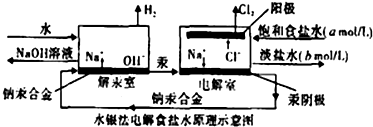 水银法电解食盐水是氯碱工业发展进程中的重要里程碑,以制得碱液纯度高、质量好而著称,其生产原理示意图如图.下列说法正确的是( )
水银法电解食盐水是氯碱工业发展进程中的重要里程碑,以制得碱液纯度高、质量好而著称,其生产原理示意图如图.下列说法正确的是( )| A、钠汞合金中钠的化合价为+1价 |
| B、电解室中产生氯气的电极为阳极,产生氢气的电极为阴极 |
| C、当阳极产生3.36 m3(标准状况)Cl2时,解汞室中生成NaOH的质量为24kg |
| D、目前氯碱生产采用离子膜法取代了水银法,其主要原因是汞有毒性,对环境有污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
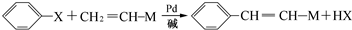 (X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下: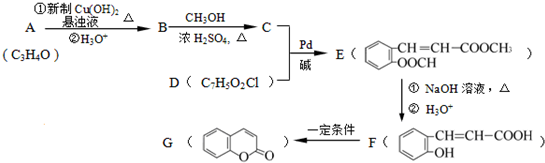
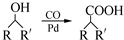 (R,R′为烃基),试写出以苯和丙烯(CH2═CH-CH3)为原料,合成
(R,R′为烃基),试写出以苯和丙烯(CH2═CH-CH3)为原料,合成 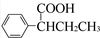 的路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
的路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
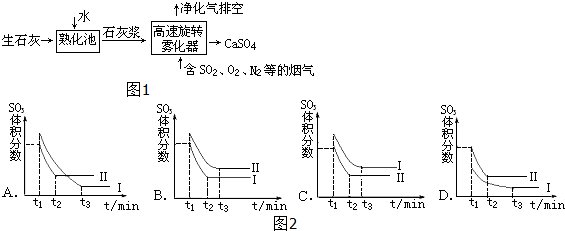
查看答案和解析>>
科目:高中化学 来源: 题型:
| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 污渍爆炸盐 | 漂白粉 |
| 产品样式 |  |  |  |  |  |
| 有效成分 或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过碳酸钠 | 消毒 |

| 实验步骤 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中,通入足量的CO2气体, | 漂白粉的漂白作用已完全失效. |
查看答案和解析>>
科目:高中化学 来源: 题型:
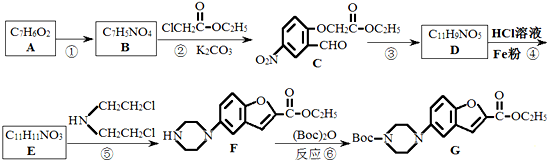
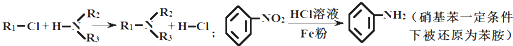
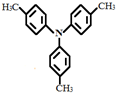 ,请设计合成路线(无机试剂及溶剂任选).
,请设计合成路线(无机试剂及溶剂任选).| O2 |
| 催化剂 |
| CH3CH2OH |
| 浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |

| △n(40℃) |
| △n(60℃) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com