
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.0.1 mol·L-1氨水中,c(OH-)=c(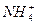 ) ) |
| B.0.1 mol·L-1NH4Cl溶液中,c(H+)=c(NH3·H2O)+c(OH-) |
C.0.1 mol·L-1NaHCO3溶液中,c(Na+)=2c(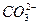 )+c( )+c(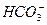 )+c(H2CO3) )+c(H2CO3) |
| D.0.02 mol·L-1盐酸与0.02 mol·L-1Ba(OH)2溶液等体积混合后,溶液的pH=13 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 和Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
和Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系: )>c(H+)>c(OH-)
)>c(H+)>c(OH-) )>c(OH-)>c(H+)
)>c(OH-)>c(H+) )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+) )>c(OH-)
)>c(OH-)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 H++
H++ 。
。 )="0.029" mol ·L-1,则25 ℃时,0.1 mol·L-1 H2SO4溶液中c(
)="0.029" mol ·L-1,则25 ℃时,0.1 mol·L-1 H2SO4溶液中c( )________(填“大于”,“小于”或“等于”)0.029 mol ·L-1,理由是__________。
)________(填“大于”,“小于”或“等于”)0.029 mol ·L-1,理由是__________。A.c(Na+)+c(H+)=c(OH-)+c(HSO-4)+2c( ) ) |
B.2c (Na+)=c( )+c(HSO-4) )+c(HSO-4) |
C.c(Na+)>c( )>c (H+)>c (OH-) )>c (H+)>c (OH-) |
D.c( )+c(HSO-4)="0.1" mol·L-1 )+c(HSO-4)="0.1" mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
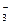 电离度大,则下列反应不正确的是()
电离度大,则下列反应不正确的是()A.Na2CO3+H2S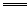 NaHCO3+NaHS NaHCO3+NaHS |
B.Na2S+H2O+CO2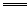 NaHS+NaHCO3 NaHS+NaHCO3 |
C.2NaHCO3+H2S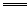 Na2S+2H2O+2CO2↑ Na2S+2H2O+2CO2↑ |
D.2NaHS+H2O+CO2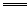 Na2CO3+2H2S Na2CO3+2H2S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
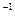 NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L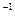
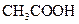 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是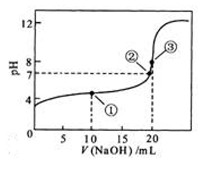
A.点①所示溶液中: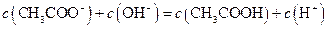 |
B.点②所示溶液中: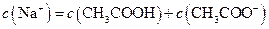 |
C.点③所示溶液中: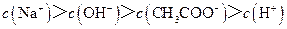 |
| D.滴定过程中可能出现: |
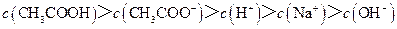
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com